Uniones químicas y propiedades de las sustancias
1. Introducción a los enlaces químicos
La mayoría de los elementos no se encuentran libres en la naturaleza sino formando parte de diferentes compuestos. Los elementos sodio y cloro, por ejemplo, están presentes en el cloruro de sodio, la sal común, NaCl. El carbono forma parte de sustancias muy conocidas, por ejemplo, dióxido de carbono, CO2 (que producimos al respirar, que utilizan las plantas en el proceso de fotosíntesis); del etanol, C2H5OH (alcohol de las bebidas, el mismo que hay en los botiquines de primeros auxilios, que se produce durante la fermentación de la glucosa de las frutas para obtener vino o sidra); de la sacarosa, azúcar de mesa, C12H22O11; del metano, CH4, componente del gas natural; entre muchísimos otros compuestos, y también se encuentra naturalmente como sustancia simple en el diamante y el grafito (mina de lápiz). Algunas preguntas que intentaremos responder durante el recorrido de este bloque son: ¿Cómo los elementos se combinan unos con otros? ¿Qué fuerzas mantienen unidos a los átomos, iguales o diferentes, en una molécula? ¿Todas las sustancias están formadas por moléculas? ¿Qué propiedades tienen estas sustancias?
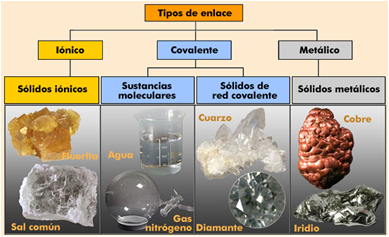
Las propiedades de las sustancias dependen en gran medida de la naturaleza de los enlaces que unen sus átomos. Existen tres tipos principales de enlaces químicos que vamos a estudiar en este bloque: enlace iónico, enlace covalente y enlace metálico. Estos enlaces, al condicionar las propiedades de las sustancias que los presentan, permiten clasificarlas en: sustancias iónicas (llamadas comúnmente SALES), covalentes (conocidas como sustancias moleculares y llamadas comúnmente MOLÉCULAS) y sustancias metálicas (llamadas METALES).
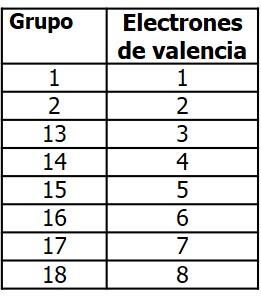
El desarrollo de la tabla periódica actual y la determinación de las configuraciones electrónicas dieron a los químicos los fundamentos para poder entender cómo se forman las sustancias (simples o compuestas, moleculares o iónicas). Recordemos que los elementos pertenecientes a un mismo grupo de la tabla periódica tienen generalmente propiedades químicas similares y sus átomos, la misma configuración electrónica externa (CEE). Esto quiere decir que presentan el mismo número de electrones en su orbital más externo (el más alejado al núcleo del átomo). Existe una estrecha relación entre el número de electrones externos y el comportamiento químico de los átomos; en particular, si se consideran los elementos representativos (grupos 1, 2 y del 13 al 18). Los electrones más externos son muy importantes ya que son los que intervienen en los enlaces químicos y se denominan electrones de valencia. Conocer el número de electrones de valencia nos ayuda a predecir de qué manera se unirá ese átomo con otro. Para los elementos representativos de la tabla Periódica, el número de grupo (en la Tabla Periódica) coincide con su número de electrones de valencia, como pueden ver en la siguiente Tabla: