Uniones químicas y propiedades de las sustancias
2. Regla del octeto
Según la regla del octeto los átomos pueden ceder electrones, aceptar electrones o compartir electrones para enlazarse con otros átomos y así adquirir la Configuración Electrónica Externa (CEE) del gas noble más próximo en la tabla periódica, y de esa manera completar con 8 electrones su orbital más externo.
¿Por qué los átomos quieren adquirir la CEE del gas noble más próximo en la Tabla Periódica (o más cercano en número atómico)? Porque los gases nobles son sustancias extraordinariamente poco reactivas. Todos ellos son monoatómicos, lo que significa que no tienen tendencia a combinarse con ningún átomo, ni siquiera con ellos mismos. Se escasa reactividad llevo a pensar que su configuración electrónica es más estable que la de otros elementos. Hoy sabemos que los átomos tienden a combinarse de manera de adquirir una configuración electrónica que les otorgue la mayor estabilidad posible. Por eso tienden a combinarse de manera de adquirir la CEE del gas noble más cercano en número atómico.
¿Por qué se unen los átomos? Lo hacen para llegar al estado de mínima energía (más estable), es decir que, cuando dos átomos se unen para formar un enlace estable se libera cierta cantidad de energía. Esa misma energía debemos entregar si queremos romper la unión química.
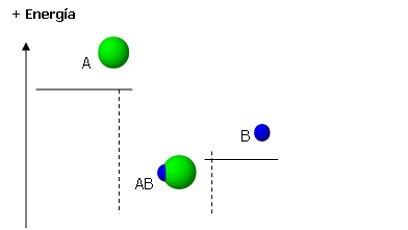
El gráfico representa la energía que presentan un átomo A y un átomo B en forma aislada en estado inicial, y la energía del compuesto AB cuando éstos átomos se enlazan por medio de una unión química. Noten que la energía del compuesto AB es menor que la energía de los átomos A y B.