Uniones químicas y propiedades de las sustancias
3. Tres tipos de uniones químicas
Veamos con mayor detalle los tres tipos de uniones químicas que vamos a aprender en esta unidad:
- Uniones Metálicas, que ocurren entre los metales
- Uniones Covalentes, que permiten la formación de moléculas
- Uniones Iónicas, que permiten la formación de compuestos iónicos que llamamos comúnmente sales.
Los átomos de los elementos metálicos, cuando no forman parte de sales u óxidos, se mantienen juntos a través de lo que llamamos uniones METÁLICAS. Los átomos de los metales tienen pocos electrones en su última capa, por lo general 1, 2 ó 3. Éstos átomos pierden fácilmente esos electrones (electrones de valencia) y se convierten en iones positivos, por ejemplo Na+, Ag+, Cu2+, Mg2+. Los iones positivos resultantes (cationes) se ordenan en el espacio formando la red metálica. Los electrones de valencia desprendidos de los átomos metálicos forman una nube de electrones que puede desplazarse a través de toda la red. En el siguiente esquema se muestra el conjunto de los iones positivos metálicos en el metal plata (Ag+), unidos mediante una nube de electrones deslocalizados (simbolizados como puntos de color azul), con carga negativa, que los envuelve:
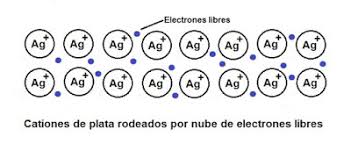
Los átomos de los elementos metálicos, además de formar uniones metálicas, también pueden formar uniones con los átomos no metálicos. Acá el acuerdo es sencillo: los metales fácilmente ceden sus electrones y los no metales no tienen ningún problema en aceptarlos. De esta manera, los átomos metálicos forman iones positivos (cationes) y los no metálicos iones negativos (aniones), que quedan unidos porque sus cargas son contrarias y SE ATRAEN FUERTEMENTE. Estas uniones se llaman IÓNICAS. En la figura de abajo se muestra como un átomo de Sodio (Na; metal) cede un electrón a un átomo de Cloro (Cl; no metal), quedando el Na con carga neta positiva (catión) unido al Cloro con carga neta negativa (anión) por medio de un enlace iónico:
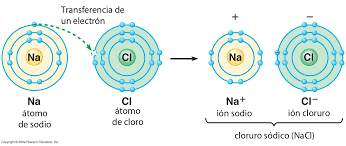
Los átomos de los elementos no metálicos llegan a completar el octeto compartiendo electrones entre ellos. Ninguno quiere perder sus electrones de valencia, pero necesitan los electrones de otros átomos para llegar a completar con 8 electrones su orbital más externo; entonces, comparten electrones. Estas uniones en las que los átomos comparten electrones se llaman COVALENTES y dan lugar a la formación de MOLÉCULAS. Moléculas como el agua (H2O), el oxígeno (O2) o el dióxido de carbono (CO2). En la figura de abajo se muestran los enlaces covalentes entre 2 átomos de Hidrógeno (H) y 1 átomo de Oxígeno (O) en la molécula de agua (H2O):
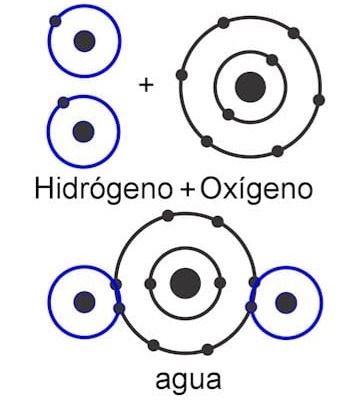
En resumen:
- en las uniones COVALENTES, los átomos implicados en el enlace COMPARTEN ELECTRONES, y este tipo de unión ocurre entre ELEMENTOS NO METÁLICOS;
- en las uniones IÓNICAS, existe una TRANSFERENCIA DE ELECTRONES de un átomo al otro, de manera que el ELEMENTO METÁLICO forma un catión (ion de carga positiva) y el ELEMENTO NO METÁLICO forma un anión (ion de carga negativa), y CATIONES Y ANIONES quedan unidos por la atracción de sus cargas contrarias;
- en las uniones METÁLICAS, participan elementos de carácter METÁLICO, que ceden fácilmente electrones y así los elementos metálicos quedan unidos por esta ¨red¨ de electrones que circulan libremente entre ellos.
Ya sea porque los átomos involucrados comparten electrones o porque ganan o pierden electrones, el "objetivo" es tener la capa electrónica más externa completa (como los gases nobles) y a esta regla, como vimos antes, la llamamos regla del octeto.