Soluciones
2. ¿Por qué algunas sustancias son solubles en determinados solventes y otras no? ¿De qué depende la solubilidad?
Para que un soluto se disuelva en un solvente, primero deben vencerse las fuerzas de atracción entre las partículas (átomos, moléculas o iones) que lo forman y separarlas de manera que las partículas de solvente sean capaces de intercalarse entre las de soluto. Por ejemplo, si disolvemos azúcar en agua, tendremos la disolución de un soluto sólido en un solvente formado por moléculas en agua.
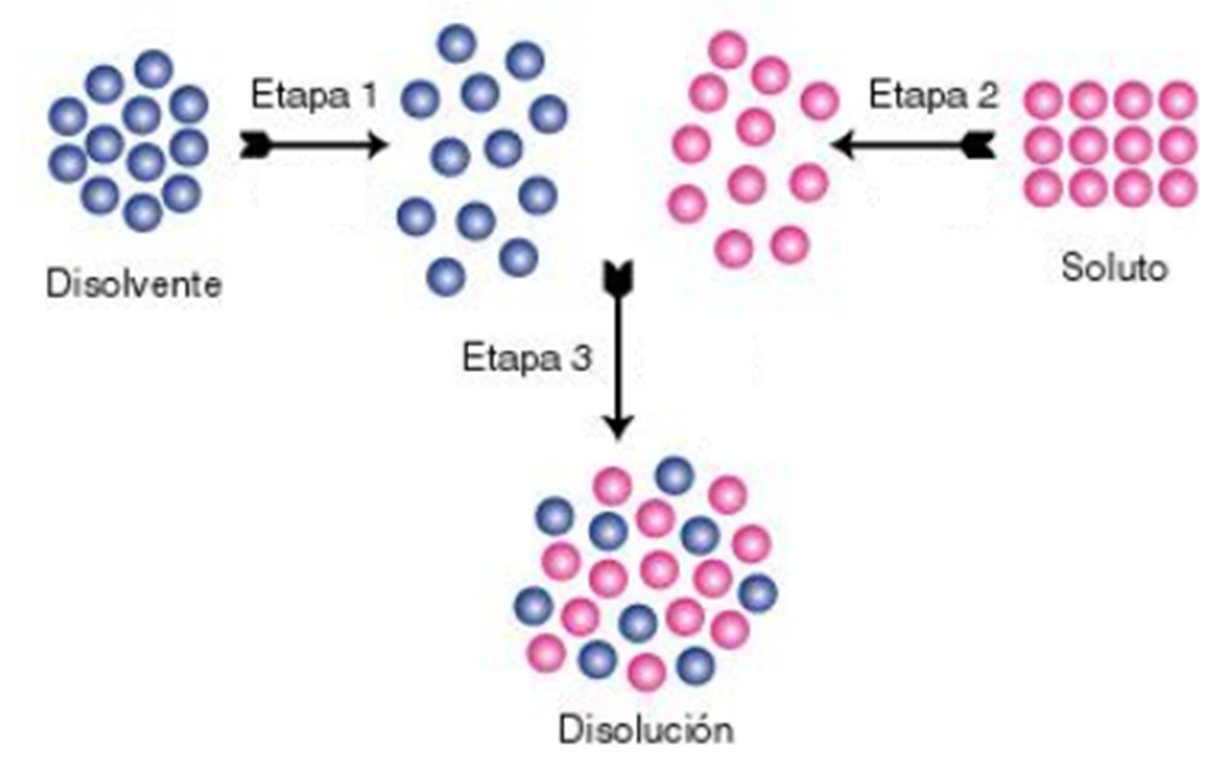
A grandes rasgos, podemos imaginar la disolución como un proceso en tres etapas: i- en la primera etapa se separan las moléculas de soluto (azúcar); ii- en la segunda se separan las moléculas de solvente (en esta etapa se necesita gastar energía para vencer las fuerzas de atracción entre las partículas se solvente); iii- se mezclan las moléculas de solvente y las de soluto. En algunos casos estos procesos ocurren en forma espontánea, en otros no. Además, estos procesos pueden ser endotérmicos (quiere decir que se necesita energía en forma de calor para que ocurran, por ejemplo, se necesita calentar la mezcla) o exotérmicos (se libera energía en forma de calor cuando ocurre la mezcla).