Soluciones
5. Distintas formas de expresar la concentración de las soluciones
Imaginemos 3 soluciones de dicromato de potasio (sal naranja) en agua, como las que se observan en la siguiente imagen:

¿Cómo podríamos diferenciarlas entre sí? ¿Cómo diferenciamos soluciones distintas que presentan los mismos componentes?
Como estarán pensando, no es posible distinguir a simple vista la diferencia entre estas soluciones. Los tres recipientes contienen soluciones del mismo soluto. Por lo tanto, la respuesta está en identificar a cada solución no por su composición, como hacemos en el caso de las sustancias, sino por su CONCENTRACIÓN: esto es, por la relación que existe (de masas o de volúmenes) entre los componentes o entre cada componente y la solución. En conclusión, la imagen de arriba muestra 3 soluciones que presentan los mismos componentes (dicromato de potasio y agua); sin embargo, estas soluciones NO son iguales entre sí, cada una presenta distinta concentración.
¿Cómo definimos la concentración de un componente en una solución?
Como la relación entre la cantidad (masa o volumen) de dicho componente, llamado soluto, y la cantidad (masa o volumen) del otro componente de la solución, llamado solvente, o la cantidad (masa o volumen) de la solución. Esto es:
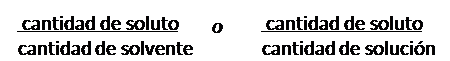
Existen diferentes formas de expresar la concentración y cada una de ellas tiene aplicaciones prácticas específicas, de modo que es habitual que se prefiera una forma de expresión a otra, según cada caso particular. Algunas formas comunes de expresar la concentración de las soluciones son las siguientes:
% m/m (porcentaje masa en masa): gramos de soluto (masa de soluto) que están presentes cada 100 g de solución.
% m/V (porcentaje masa en volumen): gramos de soluto (masa de soluto) que están presentes cada 100 mL de solución.
% V/V (porcentaje volumen en volumen): mL de soluto (volumen de soluto) que están presentes cada 100 mL de solución.
g/L: gramos de soluto (masa) presente por cada Litro (volumen) de solución.
molaridad (M): moles de soluto disueltos en 1 dm3 o 1 Litro (volumen) de solución.
molalidad (m): moles de soluto disueltos en
partes por millón (ppm): cantidad de unidades de una determinada sustancia (soluto) que hay por cada millón de unidades del conjunto.
Para reflexionar...
¿Cuál de estas maneras de expresar la concentración te resulta más familiar?