Reacciones químicas y cálculos estequiométricos
4. ¿Qué significa que las ecuaciones químicas deben estar balanceadas?
Siguiendo el Principio de conservación de las masas (propuesta por el químico Antoine Lavoisier) en todo sistema cerrado la masa se mantiene constante cualesquiera sean las transformaciones físicas o químicas que en él se produzcan. Este principio se basa en que la materia no puede ser ni creada ni destruida, entonces la sumatoria de las masas de los reactivos debe coincidir con la sumatoria de las masas de los productos. Por lo tanto, para que una reacción química refleje este principio debe estar correctamente balanceada; esto es, el número de átomos de cada clase debe ser igual del lado de los reactivos y de los productos. Dicho de otra forma, si en una reacción química ocurre un re ordenamiento de los átomos para que se formen nuevas sustancias, y los átomos tienen una cierta masa, entonces para que una reacción química cumpla el principio de conservación de las masas, el número y tipo de átomos que reaccionan inicialmente (masa inicial) deben estar al final de la reacción (masa final). ¿Están de acuerdo?
Analicemos como ejemplo la misma ecuación de oxidación del hierro que vimos antes:
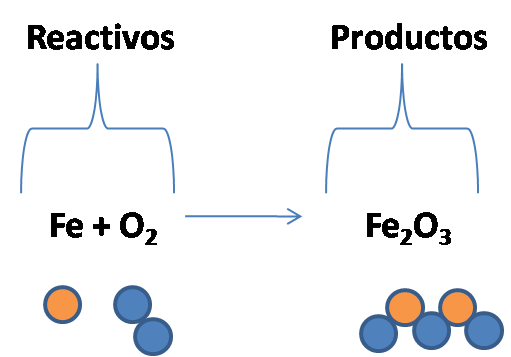
En este caso estamos representando el átomo de Fe (hierro) con una círculo naranja y el átomo de O (Oxígeno) con una círculo azul. Noten que dos átomos de Oxígeno (O) forman 1 molécula de Oxígeno (O2).
Para que la ecuación esté correctamente escrita, tiene que estar BALANCEADA, esto es, el número y tipo de átomos que están al inicio de la reacción, deben estar al final de la misma, ya que nada se crea ni se destruye, sino que se transforma.
¿Pero cómo logramos BALANCEAR la ecuación? Colocando coeficientes (números) DELANTE de la fórmula de las sustancias para lograr la igualdad de átomos de cada tipo a ambos lados de la reacción; es decir, del lado de los reactivos y del lado de los productos el número de átomos de cada tipo debe ser el mismo.
Por ejemplo:
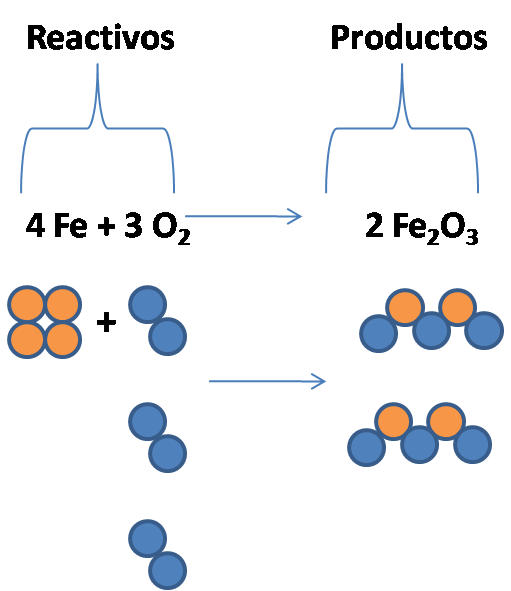
Colocando estos números delante de las fórmulas de las sustancias, logramos que tanto del lado de los reactivos como del lado de los productos haya 4 átomos de Fe (Hierro) y 6 átomos de O (Oxígeno). De esta manera la ecuación queda correctamente balanceada (cuenten el número de pelotitas naranjas y azules a ambos lados de la ecuación según indican los números DELANTE de las fórmulas moleculares).
¡OJO! Esos coeficientes o números que colocamos para igualar o balancear la ecuación solo pueden ubicarse delante de la fórmula química de cada una de las sustancias. Por ejemplo, el 3 delante de la molécula de O2, indica que se ponen a reaccionar 3 moléculas de Oxígeno: 3 O2. Esos números o coeficientes estequiométricos que colocamos para balancear la ecuación NO pueden colocarse en forma de subíndices, porque en ese caso estaríamos modificando el número de átomos de la molécula y estaríamos cambiando la identidad química de la molécula. Por ejemplo: O3, en ese caso ya no se trataría de la molécula de Oxígeno O2, sino de otra molécula llamada Ozono (O3).
Es importante destacar que los números que se colocan delante de las moléculas para balancear la ecuación es lo que tenemos que ir cambiando, hasta lograr igualar el número de átomos de cada tipo del lado de los productos y del lado de los reactivos. Este método que utilizamos para balancear esta ecuación se denomina ¨método de tanteo¨ y funciona bien para ecuaciones sencillas; sin embargo, para ecuaciones más complejas, que escapan a los objetivos de este curso, conviene muchas veces balancear las ecuaciones químicas por otro método, llamado ¨método algebraico¨.