Reacciones químicas y cálculos estequiométricos
8. Reacciones de combustión completas e incompletas
Si suponemos que, por ejemplo, se quema carbón (el combustible) en presencia de oxígeno (el comburente) estas sustancias son los reactivos o sustancias iniciales. Como resultado de este proceso se obtiene una sustancia nueva, dióxido de carbono, el producto o sustancia final. La ecuación química más sencilla que corresponde a este proceso es la siguiente:
C + O2 -----------------> CO2
En general, los combustibles que se utilizan a diario son sustancias que no están formadas sólo por carbono. El gas natural, por ejemplo es una mezcla de dos hidrocarburos: el metano (CH4) y el etano (C2H6). Cuando se produce la COMBUSTIÓN COMPLETA de estos hidrocarburos, se forman dos sustancias: dióxido de carbono (CO2) y agua (H2O). También se libera energía en forma de calor, es decir se trata de otro ejemplo de reacción exotérmica. La llama de color azul-celeste indica que la combustión es completa. Esta reacción se puede representar utilizando modelos moleculares o mediante una ecuación química (abajo):
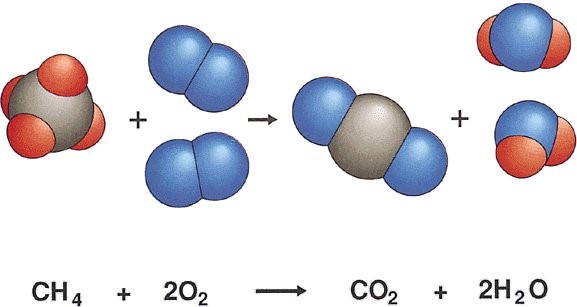
Los enlaces entre los átomos de C (representados con bolitas grises) e H (representados con bolitas rojas) del metano (CH4) y los átomos de O (representados con bolitas azules) en las moléculas de oxígeno (O2) se separan para luego formar nuevos enlaces. Es decir, durante la reacción química los átomos se reordenan (se rompen enlaces y crean nuevos enlaces) formando sustancias diferentes a las que reaccionan. En este caso la energía necesaria para romper los enlaces en las moléculas reaccionantes es menor a la que se libera al formar los enlaces en las sustancias producto de la reacción y por eso la reacción es exotérmica (es decir que se libera energía en esta reacción en forma de CALOR). Noten además que esta ecuación esta escrita en forma BALANCEADA.
Si, en cambio, la cantidad de comburente (oxígeno) disponible NO es suficiente, se produce lo que se denomina una COMBUSTIÓN INCOMPLETA, que da lugar a la producción de otro compuesto, el peligroso monóxido de carbono, cuya fórmula molecular es CO. La llama de color amarillo-naranja indica una combustión incompleta.
La ecuación será entonces: C + O2 -----------------> 2 CO
En conclusión, una combustión completa de hidrocarburos da como productos dióxido de carbono y agua, pero como vimos, pueden producirse también combustiones incompletas si la cantidad de oxígeno no es suficiente. En estos casos aparecen otros productos: el peligroso monóxido de carbono, CO, y eventualmente partículas de carbono que se desprenden y son las responsables del tiznado que aparece en las ollas. Si observas tu cocina, podrás notar que cuando la llama que produce es amarilla, se ensucian tus ollas; en cambio, si la llama que se obtiene es azul clara, esto no sucede. Efectivamente, el color amarillo se debe a la presencia de partículas de carbón que no han formado óxidos, se desprenden y se ponen incandescentes. Cuando notes que la llama de tu cocina, estufa o calefón comienza a tomar un color amarillo muy luminoso, debes destapar los quemadores (destapar los agujeritos que permiten la entrada de aire) ya que ese hecho está indicando que la combustión no es completa y que, consecuentemente es muy probable que se esté formando monóxido de carbono. Por otra parte, la combustión incompleta libera menor cantidad de calor que la completa (pero mayor cantidad de luz), por lo que para obtener una determinada cantidad de calor, se gasta más combustible que si la combustión fuese total.
¿Por qué es peligroso el monóxido de carbono?
Porque es inodoro (no tiene olor) e incoloro (no se ve) y es sumamente tóxico. Por eso todos los inviernos nos recomiendan revisar el color de la llama de estufas, quemadores, calefones, cocinas, etc. Los síntomas de la intoxicación con CO (monóxido de carbono) dependen de la cantidad de CO que existe en el ambiente. Como se trata de un gas fácilmente difusible, los niveles de CO en un ambiente cerrado aumentan rápidamente si la fuente de emisión de CO se mantiene activa. Cuando la concentración es baja, puede demorarse entre cinco y seis horas en aparecer los síntomas. Normalmente, los tejidos que necesitan mucha energía para funcionar (como el cerebro y el corazón) serían los primeros en afectarse y en mayor grado que otros.
A su vez, la falta de oxígeno puede ser tan grave como la presencia de monóxido de carbono, ¡por eso es importante mantener siempre ventiladas las habitaciones!
¡¡PARA RECORDAR!! Las reacciones de combustión pueden ser completas o incompletas; si la cantidad de oxígeno es insuficiente decimos que la combustión es incompleta, y si la cantidad de oxígeno es suficiente las reacciones de combustión son completas. En el último caso, se produce dióxido de carbono como producto y la llama que se observa es color celeste- azul; en el caso de las combustiones incompletas se produce monóxido de carbono como producto y la llama que se observa es color amarillo.