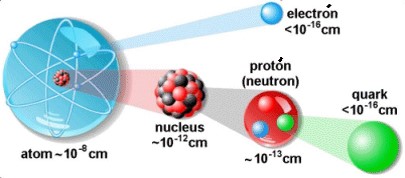
Estructura atómica
| Sitio: | Campus Claves Académica |
| Curso: | Química - EnlaceUBA |
| Libro: | Estructura atómica |
| Imprimido por: | Invitado |
| Día: | sábado, 16 de mayo de 2026, 21:05 |
Descripción
1. Entrando en tema
Desde tiempos remotos, el hombre se ha visto impulsado a examinar y a tratar de descubrir la estructura de la materia, intentando comprender todos los fenómenos que se relacionan con ella. Los antiguos pensadores griegos creían que toda la materia estaba formada por una combinación de tierra, agua, fuego y aire. Luego, entre los siglos V y VI a.C. los filósofos Leucipo y Demócrito concibieron la materia como discontinua, suponiéndola formada por pequeñas partículas indestructibles a las que llamaron ÁTOMOS, que significa indivisible o inseparable (del griego, a: privativo – tomo: cortar o dividir).
En este bloque vamos a aprender cómo es la estructura de los átomos y cuáles son las partículas subatómicas que los forman. Además conocerás algunas de las magnitudes atómicas y moleculares que permiten a los químicos resolver problemas numéricos y conceptuales, relacionados con la química.
Si te gustaría saber cómo fueron cambiando las ideas sobre la estructura de los átomos a lo largo de la historia, seguí leyendo el siguiente capítulo llamado ¨Un poco de historia sobre teoría atómica¨. En caso contrario, podes avanzar directamente hacia el capítulo: "Modelo atómico actual".
2. Un poco de historia sobre teoría atómica
En el siglo XIX, con John Dalton, comenzaron a surgir nuevas ideas acerca de la composición de la materia. La teoría atómica de Dalton se fundamentó en diversos hechos experimentales y puede resumirse en los siguientes 3 postulados:
- Los elementos están formados por partículas muy pequeñas llamadas átomos. Los átomos de un mismo elemento son idénticos entre sí y los de distintos elementos son diferentes.
- Los compuestos están formados por átomos de más de un elemento. En cualquier compuesto la relación entre el número de átomos de cualquier par de elementos presentes es un número entero o se puede expresar como una fracción simple.
- Una reacción química implica solo una separación, combinación o nueva disposición de átomos, pero éstos no se crean ni se destruyen.
A partir de la teoría de Dalton se puede definir a un átomo como la unidad básica de un elemento que puede intervenir en una combinación química. Sin embargo, una serie de investigaciones posteriores demostró que los átomos tiene una estructura interna, es decir, están formados por partículas aún más pequeñas denominadas partículas subatómicas. Algunos de los experimentos más importantes, que ampliaron el desarrollo de la teoría atómica postulada por John Dalton y permitieron postular nuevos modelos atómicos, fueron:
En 1833 Michael Faraday (inglés, 1791-1867) realizó la electrólisis del agua que consistía en hacer pasar una corriente eléctrica a través de una solución acuosa, en la cual se producía una reacción química y el resultado de esta experiencia fue la clave más importante para interpretar y entender la naturaleza eléctrica de los átomos.
En 1874, George Johnstone Stoney (irlandés, 1826-1911) reconoció el contenido de los experimentos de Faraday, y fue el primero que propuso el término “electrón” para describir la unidad fundamental de la carga eléctrica. Pero hasta 1897, no se encontró ninguna evidencia sobre la existencia y propiedades de dicha partícula. En ese año, Joseph John Thomson realizando distintos experimentos descubrió unas partículas de carga eléctrica negativa a las que años más tarde las llamó ELECTRONES. Estas partículas no dependían del material con el que trabajara, de ahí que asumió que se trataría de una partícula constituyente de toda la materia. También encontró que la masa del electrón es muy pequeña con respecto a la del átomo.
Años mas tarde, los científicos pensaron en un modelo electrónico del átomo constituido por partículas negativas (electrones) y predijeron la existencia de partículas positivas ya que la materia es eléctricamente neutra (no tiene carga eléctrica neta, por lo tanto, debe haber igual número de cargas positivas y negativas).
Realizando diferentes experimentos, Eugen Goldstein (alemán, 1850 - 1930), descubrió una corriente de partículas positivas a las que denominó PROTONES. De esta manera, se consideraba al átomo formado por partículas positivas y negativas; la dificultad consistía en saber como estaban distribuidas.
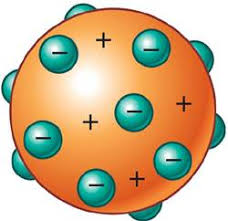
A partir de estos experimentos surgió el modelo atómico de Thomson, llamado comúnmente “modelo de budín de pasas”, un modelo de átomo compacto.
1. El modelo atómico de Thomson se puede representar de la siguiente manera:
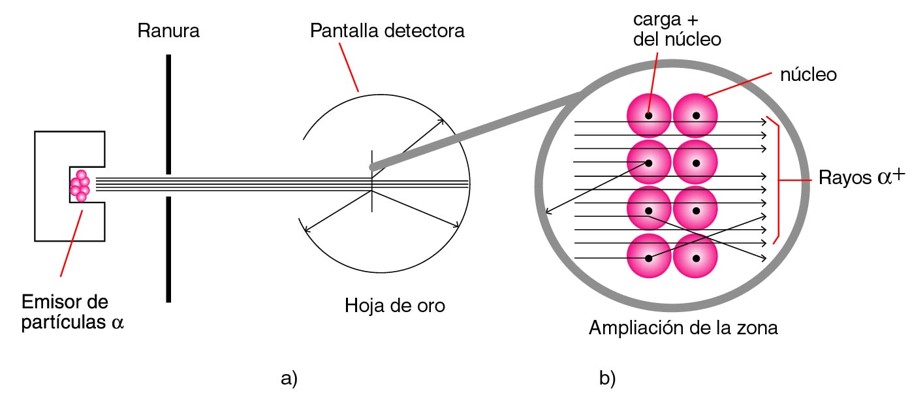
En 1910, Ernest Rutherford utilizando el fenómeno de la radiactividad en sus investigaciones, hizo incidir partículas alfa (a, masa y carga similar a los núcleos de los átomos de helio, 42He2+) sobre una lámina delgada de oro y observó con gran sorpresa que la mayoría de ellas pasaban a través de la lámina, mientras que sólo algunas se desviaban e incluso regresaban hacia la fuente emisora por la misma trayectoria (como se muestra en a). Esto permitió refutar el modelo de Thomson (átomo compacto).
Esta experiencia sirvió para demostrar cómo están distribuidas las partículas eléctricas dentro del átomo. A partir de esto, Rutherford postuló que la carga positiva del átomo está concentrada en el núcleo. Cuando una partícula alfa se acerca al núcleo, actúa una fuerza de repulsión (cargas del mismo signo se repelen) y sufre una gran desviación por tener carga del mismo signo. Supuso entonces, que la mayor parte de un átomo debe ser espacio vacío ya que la mayoría de las partículas pasaron a través de la lámina de oro con muy poca o ninguna desviación (como se muestra en b).
Rutherford concluyó diciendo lo siguiente:
- La mayor parte de la masa del átomo se encuentra concentrada en el núcleo, donde se ubican las partículas positivas;
- El radio del núcleo es 10.000 veces más pequeño que el radio atómico;
- Dado que los átomos son eléctricamente neutros, cada átomo debe tener igual número de cargas positivas y negativas;
- Los electrones se encuentran a gran distancia del núcleo. La masa del electrón es despreciable (o sea, insignificante, muy pequeña) con respecto a la masa del núcleo.
2. Modelo atómico de Rutherford se puede representar de la siguiente manera:
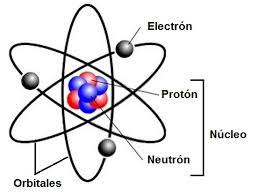
¿Por qué se cambió el modelo de Rutherford?
Este modelo se dejó de lado porque era incompatible con los conocimientos (bien corroborados) que existían en ese momento sobre electricidad: toda carga eléctrica en movimiento, emite energía. Por lo tanto, si los electrones se movían alrededor de un núcleo positivo, y perdían energía continuamente, terminarían chocando contra el núcleo. Es decir, a medida que el electrón perdía energía, la atracción que ejercía el núcleo (con carga de signo contrario) sobre él aumentaba, y en algún momento los electrones terminarían incrustándose en el núcleo.
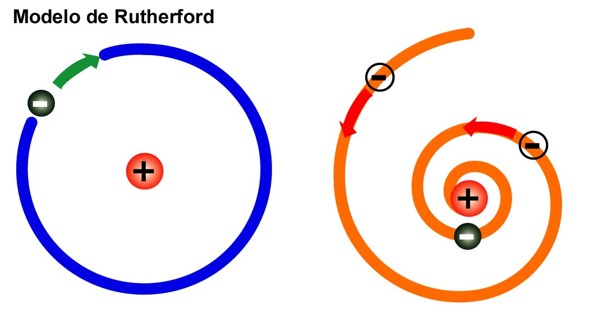
Dado que la materia existe, y la teoría sobre su composición estaba bien corroborada (átomos formados por protones y electrones), el modelo propuesto debía estar equivocado.
3. Modelo atómico de Bohr
En 1913 Niels Bohr (danés, 1885-1962) publicó una explicación teórica para el espectro atómico del hidrógeno. Basándose en las ideas previas de Max Plank, que en 1900 había elaborado una teoría sobre la discontinuidad de la energía (Teoría de los cuantos), Bohr supuso que el átomo solo puede tener ciertos niveles de energía definidos.
Bohr establece así, que los electrones solo pueden girar en ciertas órbitas de radios determinados. Estas órbitas son estacionarias, en ellas el electrón no emite energía: la energía cinética del electrón equilibra exactamente la atracción electrostática entre las cargas opuestas de núcleo y electrón.
El electrón solo puede tomar así los valores de energía correspondientes a esas órbitas. Los saltos de los electrones desde niveles de mayor energía a otros de menor energía o viceversa suponen, respectivamente, una emisión o una absorción de energía electromagnética (fotones de luz).
Las bases del modelo de Bohr fueron las siguientes:
- Los electrones en los átomos solo presentan ciertos estados energéticos estables. Así, no cualquier órbita del modelo planetario estaría permitida para el electrón;
- Los electrones son partículas cargadas, pero no emiten radiación en su viaje alrededor de núcleo, sino solamente cuando cambia el radio de su órbita.
Cuando todos los electrones de un átomo se encuentran en su estado de mínima energía, se dice que el átomo está en estado fundamental. Y los electrones ocupan los niveles energéticos más cercanos al núcleo. Cuando un electrón absorbe energía, se aleja del núcleo; “salta” a niveles de mayor valor energético. Este estado es sólo temporal y el electrón libera esa energía absorbida en forma de luz, regresando al nivel del que partió. El color de la luz emitida depende de la cantidad de energía liberada.
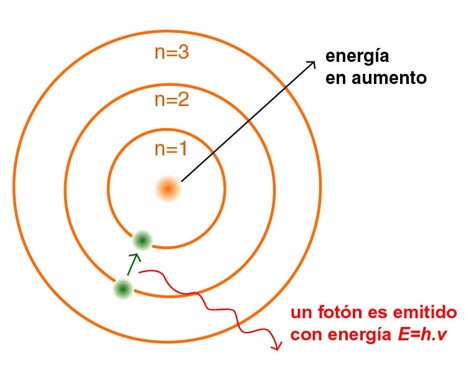
Sin embargo, el modelo atómico de Bohr también tuvo que ser abandonado al no poder explicar los espectros de átomos más complejos.
4. Teoría cuántica
Finalmente, en 1900 Max Karl Planck (alemán, 1858-1947), creador de la teoría cuántica, explicó que la energía se emite en unidades pequeñas separadas, como “paquetes”, denominadas cuantos. Así se inicia para la física la etapa conocida como mecánica cuántica y proporciona los cimientos para la investigación en lo referente a la energía atómica.
Las ecuaciones de la mecánica cuántica introducen cuatro números cuánticos que describen los estados de energía posible para los electrones y por lo tanto, la probabilidad de encontrarlos en una zona del espacio alrededor del núcleo atómico. A esta región del espacio donde es probable encontrar al electrón, se la llama ORBITAL. De esta manera, se descarta la idea de órbitas como trayectoria fija de los electrones alrededor del núcleo postulada por los modelos atómicos anteriores, para reemplazarla por una zona donde los electrones se mueven sin un camino predeterminado.
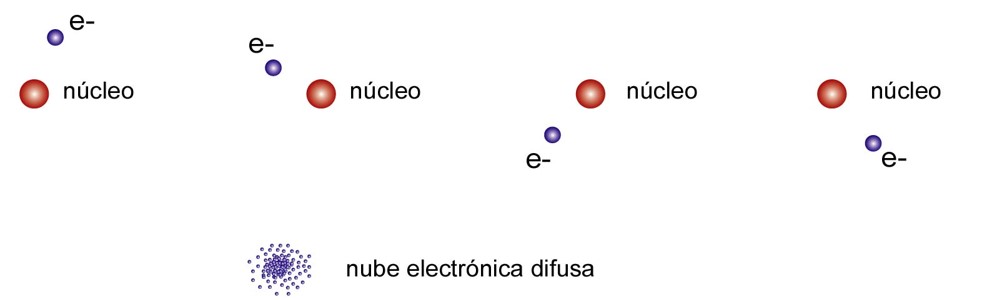
Si pudiéramos fotografiar al electrón de un átomo en un instante dado y tomásemos varias fotografías sucesivas, observaríamos al superponerlas que las posiciones del electrón nos dan una imagen difusa (nube electrónica), sin límites definidos, que nos indica que el electrón no gira en órbitas determinadas y sólo podemos conocer con cierta probabilidad la zona donde se encuentra (orbital).
Más adelante, en 1932 James Chadwick (inglés, 1891-1974) realiza una serie de experimentos cuyos resultados se podían explicar si se aceptaba la existencia de otra partícula atómica en el núcleo del átomo. Tales partículas tenían una masa muy semejante a la del protón, pero sin carga eléctrica, y fueron llamadas NEUTRONES.
3. Modelo atómico actual
En este esquema se representa como fueron evolucionando los distintos modelos atómicos hasta llegar al modelo atómico actual:

4. Número atómico y número másico
Todos los átomos se pueden identificar por el número de protones y neutrones que contienen. En química se utilizan dos números que en realidad son letras para indicarlos: el NÚMERO ATÓMICO y el NÚMERO MÁSICO.
El NÚMERO ATÓMICO identifica a los distintos elementos, ya que indica la cantidad de protones que un átomo de ese elemento tiene en su núcleo y se representa con la letra Z. Este número, también se utiliza para ordenar los elementos en la Tabla Periódica.
En el núcleo de los átomos, además de protones hay neutrones. La suma del número de protones y neutrones en el núcleo de un átomo recibe el nombre de NÚMERO MÁSICO y se simboliza con la letra A.
La forma aceptada para anotar el número atómico y el número másico de un elemento X es la siguiente:
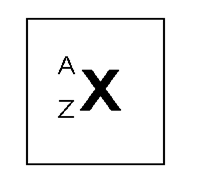
Número atómico (Z) = Número de protones
Número másico (A) = Número de protones + Número de neutrones
A = Z + Número de neutrones (n)
Por lo tanto, el número de neutrones se puede calcular así:
n = A - Z
A partir de aquí haremos referencia muchas veces a los elementos con sus símbolos químicos. Para que vayas familiarizándote con este tipo de lenguaje, es conveniente que tengas siempre a mano una Tabla periódica para consultar. Haciendo click aquí podes encontrar una Tabla Periódica Web Interactiva.
En el siguiente video les contamos muy brevemente cómo usar esta Tabla Periódica Web Interactiva y cómo están organizados los Elementos (este tema se trata en mayor profundidad en el bloque llamado Clasificación Periódica).
>
5. Isótopos
Como habrás visto en la tabla periódica figura un solo casillero para cada elemento, sin embargo no todos los átomos de un elemento dado tienen la misma masa. La mayoría de los átomos presentan ISÓTOPOS, átomos que tienen el mismo número atómico (Z) pero diferente número másico (A). Por ejemplo, existen 3 isótopos del Hidrógeno que pueden observar en el siguiente esquema:
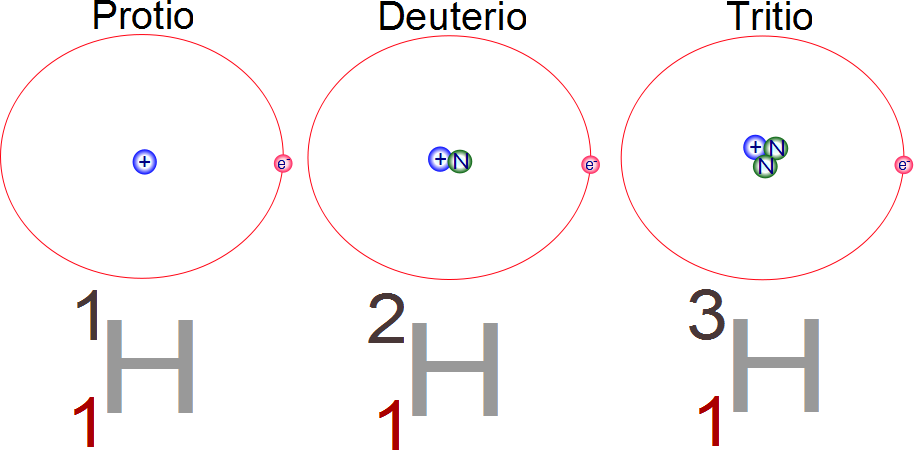
Uno de ellos se conoce como Protio o Hidrógeno, es el más abundante en la naturaleza, tiene 1 protón y no tiene neutrones. El isótopo llamado Deuterio tiene 1 protón y 1 neutrón, y el llamado Tritio tiene 1 protón y 2 neutrones. Con excepción del Hidrógeno que tiene un nombre diferente para cada uno de sus isótopos, los isótopos de los demás elementos se identifican por su número másico o número de masa.
Para reflexionar..
Las propiedades químicas de los átomos de un elemento dado están determinadas, fundamentalmente, por sus protones y electrones. En condiciones normales, los neutrones no participan en los cambios químicos. Teniendo en cuenta esto, si tuvieras que predecir el comportamiento químico de los isótopos del hidrógeno, ¿dirías que formarán el mismo tipo de compuestos y reaccionarán de manera similar o no?
6. Masa atómica
¡Sigamos trabajando con la Tabla Periódica de los Elementos! Como se mostro en el video anterior, debajo del NOMBRE de cada ELEMENTO figura la MASA ATÓMICA: es decir, la masa de los átomos que pertenecen a ese elemento. Debemos aclarar que no es la masa de un átomo en particular, sino el PROMEDIO de la masa de los distintos isótopos que se encuentran en la naturaleza para cada elemento, TENIENDO EN CUENTA SU ABUNDANCIA RELATIVA. Deberíamos llamarla MASA ATÓMICA PROMEDIO, pero en la práctica la llamamos MASA ATÓMICA. Veamos un ejemplo:
El cloro tiene dos isótopos: Cl-35 y Cl-37. Si la masa atómica del cloro fuese simplemente el promedio de masas de sus isótopos 35 y 37, sería 36 no? Pero si se fijan en la tabla periódica la masa atómica del Cloro es 35,45. ¿Por qué? La respuesta tiene que ver con el hecho que diferentes isótopos tienen distinta abundancia relativa, es decir que algunos isótopos naturalmente son más abundantes en la Tierra que otros. En el caso del cloro, el cloro-35 tiene una abundancia relativa de 75,5% mientras que el cloro-37 tiene una abundancia relativa de 24,5%. Observa que la abundancia relativa es un porcentaje y por lo tanto la abundancia relativa de todos los isótopos estables distintos de un elemento suman 100%.
Entonces, teniendo en cuenta su abundancia relativa calculamos el promedio ponderado de masas atómicas de los isótopos del cloro de la siguiente manera= 35 uma x 75,5/100 + 37 uma x 24,5/100 = 35,45 uma. Esta masa atómica es la que apareceen la tabla periódica para el cloro.
¡Ojo! Si bien son palabras similares no es lo mismo el NÚMERO MÁSICO y la MASA ATÓMICA.
En la Tabla Periódica NO se indica el número másico (que corresponde a la suma de protones más neutrones y por lo tanto SIEMPRE ES UN NÚMERO ENTERO); en cambio, SÍ se indica la masa atómica que, como vimos es un promedio de la masa de todos los isótopos teniendo en cuenta su abundancia relativa, por eso se trata siempre de un número con decimales. ESTE VALOR SÍ LO PODEMOS ENCONTRAR EN LA TABLA PERIÓDICA, como pueden ver en la siguiente imagen:
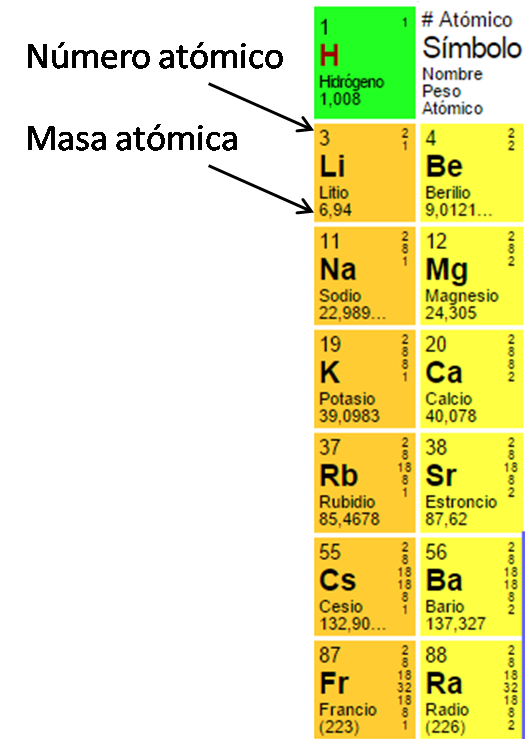
Tengan en cuenta que como las partículas subatómicas que aportan a la masa de los átomos son los NEUTRONES y los PROTONES y su masa es 1 uma, en general la MASA ATÓMICA de un átomo suele ser un número muy cercano a su NUMERO MÁSICO.
También es importante notar que las masas de los átomos son muy pequeñas comparadas con las masas que manejamos habitualmente. Esto hace imposible medirlas con las balanzas convencionales y en las unidades habituales como kg, g e incluso mg que resultan demasiado grandes para que sean de utilidad. Este tema se verá en profundidad en otro bloque, pero te adelantamos que como NO es posible pesar un solo átomo con ningún instrumento hasta la fecha. Por eso para determinar la masa de los mismos, se tomo como PATRÓN de referencia al isótopo más abundante del carbono (C-12), asignando a su masa un valor de doce unidades de masa atómica (uma). Por lo tanto, las masas atómicas tal como figuran en la Tabla periódica corresponden a masas atómica relativas (que se abrevia como Ar). Al ser relativas, estos números indican cuantas veces es mayor la masa de un átomo en relación a la unidad de masa atómica. Veamos un ejemplo:
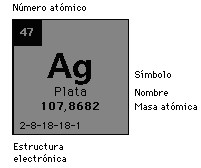
Por ejemplo, la masa atómica de la plata es 107,8682 (sin unidades), es decir, que un átomo de plata es 107,8682 veces más pesado que 1 uma o que un átomo de plata pesa 107,8682 uma.
7. ¡Trabajemos con un simulador!
Hagamos un repaso de los puntos importantes que vimos hasta aquí:
-
Los átomos que tienen el mismo número de protones pero diferente número de neutrones se llaman isótopos.
-
Los isótopos tienen distintas masas atómicas.
-
La abundancia relativa de un isótopo es la fracción en que ese elemento existe en la Tierra con una masa atómica específica.
-
La masa atómica es el promedio ponderado de masas que se calcula al multiplicar la abundancia relativa de cada isótopo por su masa atómica y luego sumar todos los productos.
Les proponemos ahora una actividad con un simulador para comprender mejor los conceptos planteados. En el siguiente esquema podes ver cómo usar el simulador y qué variables podes controlar:

El objetivo es que uses el simulador para aprender a diferenciar un isótopo de otro y para entender cómo la abundancia se relaciona con la masa atómica promedio de un elemento. Desde aquí pueden acceder al simulador, clickeando en ISÓTOPOS:
Utilizando el simulador, prueben construir los siguientes pares de isótopos:
1. Carbono A=12 ; Carbono A= 14
2. Oxígeno A= 14 ; Oxigeno A= 16
3. Nitrógeno A= 14; Nitrógeno A= 15
Entre cada par de isótopos comparen y respondan:
¿Cuántos protones, neutrones y electrones tiene cada uno? ¿Cuál es más abundante en la naturaleza?
8. Iones, cationes y aniones
Cuando los átomos presentan igual número de protones (partículas con cargas +, positivas) que de electrones (que presentan cargas -, negativas) son eléctricamente NEUTROS. Como en el caso de los átomos que construyeron con el simulador. Pero los átomos no siempre son NEUTROS, también pueden tener carga neta y entonces se denominan IONES.
Cuando los átomos PIERDEN o GANAN electrones se transforman en partículas con carga neta llamados IONES. En la imagen de abajo los electrones se representan en verde. Fíjense que:
- Si un átomo GANA 1 o más electrones su carga neta es negativa (porque gana cargas negativas). Los iones con carga NEGATIVA se denominan ANIONES.
- Si un átomo PIERDE 1 o más electrones su carga neta será positiva (porque pierde cargas negativas). Los iones con carga POSITIVA se denominan CATIONES.
En conclusión, lo que siempre GANAN O PIERDEN LOS ÁTOMOS SON ELECTRONES (partículas con carga negativa).

En resumen, los CATIONES TIENEN CARGA POSITIVA y LOS ANIONES TIENEN CARGA NEGATIVA, como pueden ver en el siguiente ejemplo:

- Recuerden que siempre son los ELECTRONES los que se ganan o pierden y NO los protones.
- La modificación en el número de protones en un átomo significa la transformación de un elemento en otro. Esto ocurre durante las reacciones nucleares, en las estrellas, en los reactores nucleares o durante una explosión atómica.
Veamos como se escriben por convención los átomos neutros vs los iones con carga neta:
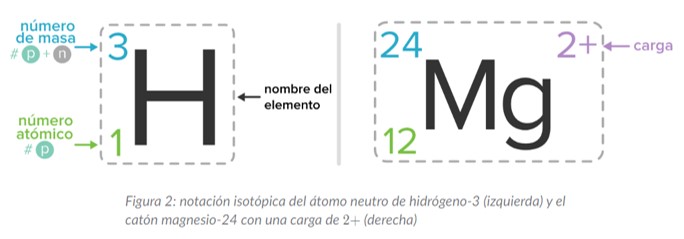
Más ejemplos:

9. Autoevaluación
Para seguir pensando y practicando los conceptos que vimos en este bloque, te proponemos realizar la siguiente actividad de auto-evaluación, a la que pueden acceder haciendo clic en Cuestionario.
|
Si no tenés un usuario creado en este campus no podés hacer las autoevaluaciones. Te dejamos las instrucciones para poder realizarlas:
|