Clasificación periódica
| Sitio: | Campus Claves Académica |
| Curso: | Química - EnlaceUBA |
| Libro: | Clasificación periódica |
| Imprimido por: | Invitado |
| Día: | domingo, 17 de mayo de 2026, 08:16 |
Tabla de contenidos
- 1. Antes de empezar... Hagamos un repaso
- 2. Un poco de historia sobre la Tabla Periódica
- 3. Organización de los Elementos en la Tabla Periódica.
- 4. Veamos un poco más en detalle cómo usar la Tabla Periódica de los Elementos
- 5. Propiedades periódicas de los Elementos
- 6. Radio atómico
- 7. Electronegatividad
- 8. Energía de ionización
- 9. ¡Trabajemos con un simulador!
- 10. Autoevaluación
- 11. ¿Nos regalás 5 minutos?
1. Antes de empezar... Hagamos un repaso
En este bloque vamos a aprender cómo están clasificados los elementos en la Tabla Periódica y cómo se lee la información que ofrece la Tabla, ¡qué tiene un montón de información!
Para entender bien cómo está construida la tabla, primero hagamos un repaso sobre estructura atómica.
Recordemos que los átomos están constituidos por distintas partículas subatómicas: los PROTONES (que tienen carga positiva), los NEUTRONES (que no tienen carga) y los ELECTRONES (cuya carga es negativa). Los protones y los neutrones forman el núcleo del átomo y tienen una masa similar, mientras que los electrones tienen una masa mucho más pequeña que la de los neutrones y protones, y están fuera del núcleo, formando parte de los orbitales extra nucleares.
Por otro lado, recordemos la identidad de los átomos esta definida por la cantidad de protones que se hallan en el núcleo, es decir, su número atómico o Z. Toda especie química que tenga el mismo número de protones en el núcleo corresponde al mismo tipo de elemento, aunque tenga distinto número de neutrones (como los isótopos) o de electrones (como los iones que derivan de un átomo).
El número másico o A indica la suma de protones y neutrones que hay en el núcleo de un átomo, y por lo tanto sirve para identificar distintos isótopos.
En el bloque correspondiente a estructura atómica, vimos algunos ejemplos de isótopos del carbono: el carbono 12 (12C), que es el más abundante en la naturaleza, el carbono 13 (13C) y el carbono 14 (14C). El 14C es bastante característico. No es una forma estable del carbono, por lo que se va desintegrando con el tiempo. Cuando un isótopo no es estable y se desintegra con el tiempo, se dice que es radiactivo. Aprovechando esta propiedad se puede conocer la edad de objetos formados por átomos de carbono de hasta 45 mil años!
Si te gustaría saber cómo fue cambiando la Tabla Periódica a lo largo de la historia, seguí leyendo el siguiente capítulo llamado ¨Un poco de historia sobre la Tabla Periódica¨. En caso contrario, podes avanzar directamente hacia el capítulo: "Organización de los Elementos en la Tabla Periódica".
2. Un poco de historia sobre la Tabla Periódica
En el siglo XIX los químicos tenían una idea vaga de los átomos y las moléculas, y no conocían como estaban formados los átomos. Las primeras tablas periódicas fueron construidas usando como base las estimaciones hechas sobre los pesos atómicos (lo que ahora llamamos masa atómica). A continuación sólo veremos dos ejemplos de las tablas que se han propuesto en los inicios de la historia de la química.
Una de las primeras tablas la propuso John A. Newlands (británico, 1837-1898), quien ordenó los elementos de acuerdo con sus pesos atómicos y vio que cada ocho elementos se repetían las propiedades. Por ejemplo, el octavo elemento, tenía propiedades similares al primero; el segundo al noveno y así sucesivamente. Las octavas de Newlands, parecían indicar una relación entre los elementos similar a la que se da entre las notas musicales.
Este ordenamiento resultó inadecuado para aquellos elementos que tenían peso atómico mayor que el del Calcio (Ca) y esta investigación no fue aceptada por la comunidad científica.
En el año 1869, el químico ruso Dimitri Mendeléiev (1834-1907) y el químico alemán Julius Lothar Meyer (1830-1895) propusieron cada uno por su cuenta un ordenamiento de los elementos teniendo en cuenta su masa atómica creciente y dispuestos de tal manera que sus propiedades químicas eran semejantes entre dichos elementos.
La confianza de Mendeleiev en su trabajo, lo llevó a predecir las propiedades de varios elementos que aún no se habían descubierto. Éstos debían ocupar los huecos que quedaban en su tabla luego de “acomodar” los elementos conocidos en su época. Por ejemplo, propuso la existencia de un elemento llamado EKA SILICIO (eka proviene del sánscrito y significa primero). Cuando se descubrió el Germanio en 1866 sus propiedades coincidían con las indicadas por Mendeleiev para el eka-silicio. También predijo las propiedades del escandio (Sc), al que llamó eka-boro.
Esta tabla fue modificada en diversas oportunidades. A medida que se descubrían nuevos elementos, debían irse incorporando y también hubo otras modificaciones mucho más trascendentes. En 1914 H. Moseley (1887-1915) determinó el número atómico de los elementos y comprobó que si se colocaban los elementos por orden creciente de su número atómico, todos quedaban situados en el lugar requerido por el criterio de semejanza de propiedades.
La ley periódica se enuncia así en la actualidad: cuando los elementos se colocan en orden creciente de su número atómico, tiene lugar una repetición periódica de ciertas propiedades físicas o químicas de aquéllos. El origen de la periodicidad en las propiedades químicas de los elementos radica en la configuración de sus electrones más externos (llamados electrones de valencia), y ésta se repite periódicamente.

Imagen de Dimitri Mendeleiev (izquierda) y foto de la Tabla original escrita de puño y letra por Mendeleiev (derecha).
3. Organización de los Elementos en la Tabla Periódica.
En la Tabla Periódica actual los elementos químicos se encuentran ordenados de acuerdo con su numero atómico (Z) creciente de izquierda a derecha y de arriba hacia abajo. Los elementos presentes en la Tabla se pueden clasificar de diferentes maneras, que veremos a continuación.
La Tabla actualmente está organizada en:
- grupos (18 columnas) que se numeran del 1 al 18, o con números romanos y un letra A o B,
- períodos (8 filas) numerados de 1-8.
Los elementos que están en el mismo grupo (es decir, en la misma columna) tienen igual número de electrones de valencia, que son los electrones que están en el orbital más externo y los que participarán de las uniones químicas (tema que desarrollaremos en otro bloque). Por esa razón los elementos de un mismo grupo, es decir que están en una misma columna, presentan propiedades químicas semejantes, y se dice que forman parte de una misma FAMILIA. Algunas de estas familias tienen nombres propios, como por ejemplo:
- los elementos del grupo IA o 1 que se llaman Metales Alcalinos,
- los del grupo IIA o 2 que se denominan Metales Alcalinos Térreos,
- los del grupo VIIA o 17 que son los llamados Halógenos,
- los del grupo VIIIA o 18 son llamados Gases Nobles o Inertes.
Como dijimos anteriormente en la Tabla los elementos están ordenados por su Z (número atómico), desde el elemento de Z = 1 (Hidrógeno) en adelante (leyendo de izquierda a derecha y de arriba hacia abajo) y se pueden clasificar de distintas maneras. Una de las formas más comunes de clasificación es según sus propiedades químicas como:
- Metales,
- No metales y
- Metaloides.
Una ACLARACIÓN IMPORTANTE: si bien el Hidrógeno está ubicado en el grupo 1 o IA, NO es un metal alcalino. El Hidrógeno es un NO METAL, pero esta ubicado allí porque su Z= 1. En la imagen de abajo pueden ver cómo a los elementos coloreados según esta clasificación:

Existe también otra clasificación de los elementos según el subnivel (s, p, d ó f) en el que ingresa el electrón diferencial; esto es, como los elementos están ordenados según su número atómico, cada elemento difiere del anterior por un protón y por ende por un electrón que se denomina electrón diferencial. Siguiendo esta regla los elementos se clasifican en:
- Elementos Representativos, los que ubican su electrón diferencial en el subnivel s o p;
- Elementos de Transición, los que ubican su electrón diferencial en el subnivel d,
- de Transición Interna, los que ubican su electrón diferencial en el subnivel f.
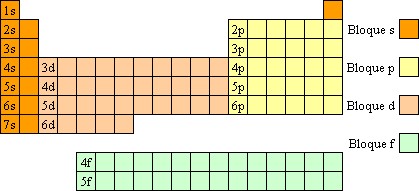
Existen los bloques:
s que abarca los grupos 1 y 2 y el elemento He;
p que abarca los grupos
d que abarca los grupos
f que abarca dos filas, la de los lantánidos y los actínidos.
Como se mencionó antes, este criterio permite clasificar los elementos en: representativos, de transición y de transición interna, como se muestra en el esquema de abajo:
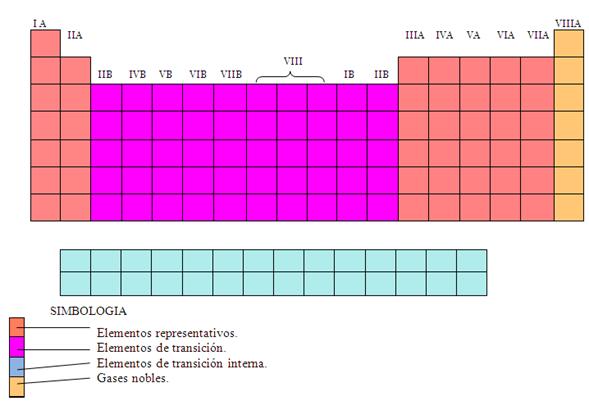
Así la distribución de familias de elementos dentro el sistema periódico es:
• Elementos representativos formados por:
Alcalinos: Grupo IA;
Alcalinotérreos: Grupo IIA Térreos;
Boroideos: Grupo IIIA;
Carbonoideos: Grupo IVA;
Nitrogenoideos: Grupo VA;
Anfígenos: Grupo VIA;
Halógenos: Grupo VIIA;
Gases nobles o inertes: Grupo VIIIA.
• Elementos de transición formados por los grupos IIIB, IVB, VB, VIB, VIIB, VIIIB (que incluye tres columnas), IB y IIB. Se sitúan en el centro del Sistema Periódico.
• Elementos de transición interna formados por las familias de Lantánidos y Actínidos, de 14 elementos cada una. Se colocan en dos filas habitualmente fuera del entorno general.
• El hidrógeno queda fuera de estas consideraciones, y por tener un solo electrón que está alojado en el orbital 1s, se coloca encima del grupo de Alcalinos IA.
4. Veamos un poco más en detalle cómo usar la Tabla Periódica de los Elementos
Lxs invitamos a conseguir una Tabla Periódica propia impresa en papel y a tenerla enfrente suyo mientras miran este video explicativo, así pueden anotar en ella lo que necesiten recordar y guardarla para su uso personal. ¡Se consiguen en cualquier librería!
Para saber más sobre la Tabla periódica....
El 2 de noviembre de 2019 la Organización de Naciones Unidas proclamó el año 2019 como el Año Internacional de la Tabla Periódica de los Elementos Químicos. Observando que el año 2019 coincide con los aniversarios de una serie de hitos importantes en la historia de la tabla periódica: en particular, con la creación de la tabla periódica por Mendeleev hace 150 años; el aislamiento del arsénico y el antimonio por Jabir ibn Hayyan hace unos 1200 años; el descubrimiento del fósforo hace 350 años; la publicación de una lista de 33 elementos químicos clasificados en gases, metales, no metales y térreos por Lavoisier en 1789; el descubrimiento de la ley de las tríadas por Döbereiner en 1829 y el descubrimiento del francio por Marguerite Perey en 1939…
A su vez, el 23 de noviembre de ese mismo año, la ingeniera química Teresa Valdés-Solís publicó en la plataforma Naukas el artículo La Tabla Periódica de las Científicas, en el que proponía una especial tabla periódica compuesta por nombres de mujeres científicas. Podes acceder a dicha tabla para conocer el papel de distintas mujeres en la ciencia haciendo click aquí. Desde esa página podes hacer click sobre el nombre o cada uno de los símbolos para encontrar la historia de cada una de estas mujeres.
5. Propiedades periódicas de los Elementos
Como se menciona en el video, los períodos se designan por números correlativos del 1 al 7. En ellos los elementos presentan propiedades diferentes. Observen que los elementos del mismo período tienen sus electrones más internos ordenados como el gas noble del período anterior. Los elementos de un período determinado se caracterizan por tener electrones en el mismo nivel más externo, que es precisamente el número que designa cada período. Así, los elementos del período 1 tienen electrones sólo en el nivel 1, los del período 2 tienen electrones ocupando hasta el nivel 2, los del tercer período tienen electrones hasta el nivel 3, y así sucesivamente.
Los grupos se designan mediante números correlativos del 1 al 18. Los elementos que componen cada grupo tienen, con escasas excepciones, similares propiedades químicas, debido a que todos coinciden en su configuración electrónica de los electrones de valencia.
Como ya mencionamos, algunas propiedades físicas y químicas se repiten con cierta regularidad a lo largo de los grupos y los períodos. La razón de su regularidad reside en la configuración electrónica y en el número atómico del elemento.
A continuación veremos algunas de las propiedades periódicas más importantes: el radio atómico, la energía de ionización y la electronegatividad.
6. Radio atómico
El tamaño del átomo es difícil de definir. No obstante, como los átomos no suelen presentarse aislados, el valor que se asigna en la práctica al radio atómico es la mitad de la distancia entre los núcleos de dos átomos iguales enlazados entre sí.
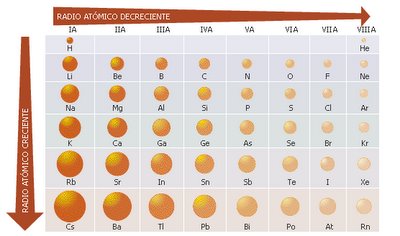
- En un período, al aumentar el número atómico, disminuye el radio atómico. Al aumentar el número atómico de los elementos de un mismo período, se incrementa la carga nuclear efectiva sobre el electrón más externo y el número de niveles ocupados no varía. En consecuencia, aumenta la intensidad de la atracción entre el electrón y el núcleo, por lo que disminuye la distancia entre ellos.
- En un grupo, al aumentar el número atómico, aumenta el radio atómico. Al aumentar el número atómico de los elementos de un grupo, se incrementa el número de niveles ocupados, mientras que la carga nuclear efectiva sobre el electrón más externo es la misma. En consecuencia, aumenta el radio atómico.
7. Electronegatividad
La electronegatividad de un elemento se define como la tendencia relativa de sus átomos para atraer los electrones de otros átomos con los que están enlazados.
En 1939 L. Pauling (1901-1994) estableció una escala arbitraria de electronegatividades, asignando al átomo más electronegativo, el de flúor, el valor 4,0 y, a partir de él, el de todos los demás.
Existen átomos como los no metales (especialmente el nitrógeno, el oxígeno y los halógenos (elementos del grupo 17: F, Cl, Br, I) que tienen una tendencia fuerte a atraer electrones. En cambio, los metales alcalinos y alcalinos térreos tienen bajas electronegatividades.
En el esquema de abajo se puede ver cómo varía la electronegatividad de los elementos de la tabla periódica. En este esquema la electronegatividad de cada elemento figura debajo de su símbolo. En las Tablas impresas el valor de electronegatividad suele figurar en el margen superior derecho dentro del cuadrante de cada Elemento:

La electronegatividad aumenta de izquierda a derecha y es mayor en los primeros períodos que en los últimos.
8. Energía de ionización
Cada elemento tiene una determinada energía de ionización, que es la energía necesaria para sacarle un electrón al átomo y formar un ión de carga positiva, es decir, un catión. Si tuviéramos que ponerle un precio a los electrones, podríamos decir que los elementos con alta energía de ionización tienen electrones más "caros" y por lo tanto hay que poner más energía para sacárselos. Por lo tanto, los elementos con alta energía de ionización tienen tendencia a formar aniones; es decir, tienen tendencia a GANAR ELECTRONES. Ejemplos de estos elementos son los NO METALES.
Por el contrario, los electrones de los metales alcalinos y alcalinos térreos son muy "baratos": están interesados en PERDER ELECTRONES. Sus energías de ionización son muy bajas y tienen mucha tendencia a formar cationes.
La energía de ionización y la electronegatividad son magnitudes útiles para predecir el tipo de unión química que se dará entre dos átomos (tema que trataremos en detalle en el bloque llamado: ¨Uniones químicas y propiedades de las sustancias¨).
En el siguiente esquema pueden ver cómo varía la energía de ionización para los elementos en la Tabla Periódica:

La energía ionización, al igual que la electronegatividad, aumenta de izquierda a derecha y es menor en los últimos períodos comparado con los primeros.
9. ¡Trabajemos con un simulador!
Vamos a trabajar con un simulador para construir los átomos de la Tabla Periódica y repasar los siguientes conceptos:
- El número de protones que esta presente en el núcleo de cada átomo (que llamamos número atómico y se simboliza con la letra Z) es lo que identifica a cada elemento; es decir, todos los átomos que tienen 1 protón en su núcleo corresponden al elemento Hidrógeno (H), todos los átomos que tienen 2 protones en su núcleo corresponden al elemento Helio (He), etc.
- Los átomos que tienen el mismo número de PROTONES pero diferente número de NEUTRONES se llaman ISÓTOPOS.
- Los suma del número de PROTONES y NEUTRONES en el núcleo del átomo corresponde al NÚMERO MÁSICO (que designamos con la letra A), porque estas partículas son las que aportan masa a los átomos.
Una de las cosas que vamos a ver al construir los átomos de los elementos de la Tabla Periódica con este simulador, es que no todos los isótopos de los elementos son igual de estables. Por ejemplo, el átomo de Hidrógeno con 1 protón es ESTABLE, su isótopo que tiene 1 protón y 1 neutrón es ESTABLE, pero el isótopo que tiene 1 protón y 2 neutrones es INESTABLE.
Además este simulador los va a ayudar a aprender los símbolos de los Elementos que vimos previamente en la Tabla Periódica y a entender en qué se diferencian los Elementos de la Tabla entre sí.
ACLARACIÓN: Para poder realizar estas actividades es importante tener claros los conceptos del bloque llamado ¨Estructura Atómica¨.
En la primer pantalla del simulador llamada ÁTOMOS, pueden construir átomos y determinar cómo se establece la identidad, la carga neta y la masa de un átomo o ion. En el siguiente esquema pueden ver cómo usar el simulador y qué variables podes controlar:
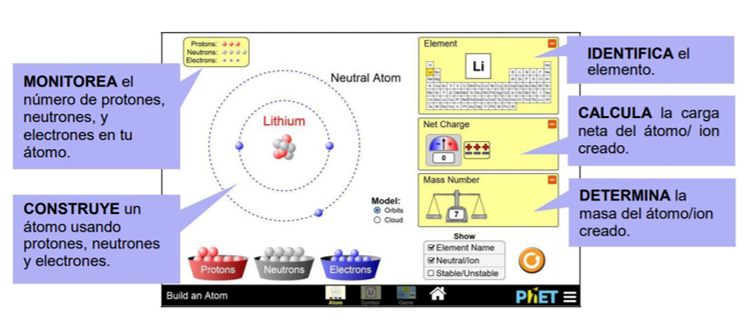
En la segunda pantalla del simulador llamada SÍMBOLO pueden interpretan símbolos químicos al construir átomos usando protones, neutrones y electrones. En el siguiente esquema pueden ver cómo usar el simulador y qué variables podes controlar:
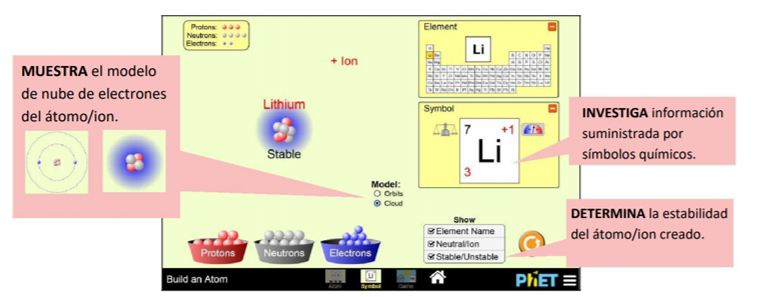
Ahora elegí la pantalla ÁTOMO en primer lugar y luego la pantalla SÍMBOLO del simulador:
Desde la pantalla ÁTOMO del simulador pueden realizar las siguientes actividades:
1) CONSTRUYAN un átomo que tenga 9 protones y 10 neutrones. INDIQUEN cuál es su:
- Número atómico Z = ________
- Número másico A = _______
- Su Símbolo:
2) CONSTRUYAN un átomo que tenga número atómico (Z) = 6 y número másico (A) = 12. INDIQUEN su número de:
- Protones: _____________
- Electrones (para que sea un átomo NEUTRO): ___________
- Neutrones: _________
- Su Símbolo:
3) CONSTRUYAN un átomo que tenga 5 neutrones y su número másico sea 9. Indiquen:
- Su número atómico Z = ___________
- Su nombre: _____________________
- Su símbolo: _____________________
Desde la pantalla SÍMBOLO pueden realizar las siguientes actividades:
4A) Construyan átomos de Helio (He), con:
- 2 protones, 1 neutrón, 2 electrones
- 2 protones, 2 neutrones, 2 electrones
- 2 protones, 3 neutrones, 2 electrones
4B) Indiquen para cada uno de los isótopos de He su Z, A y la carga neta del átomo.
4C) ¿Todos los isótopos del He tienen igual estabilidad? (para analizar este punto deben hacer click donde dice MOSTRAR: ESTABLE/INESTABLE).
4D) ¿Por qué todos los átomos que construyeron son neutros? Ahora sin importar el número de NEUTRONES, prueben con el simulador como varía la carga neta de los átomos que construyeron si el número de electrones es MAYOR al número de protones. ¿Qué carga neta tendrán los átomos?
4E) Y si el número de protones es MENOR que el número de electrones, ¿qué carga neta tendrán los átomos?
4F) A partir de las actividades 4D y 4E, ¿pueden sacar alguna conclusión general? Escriban una regla para construir un átomo neutro (con carga neta 0), un ión con carga neta positiva y un ión con carga neta negativa.
5) Todo lo que nos rodea está formado por diferentes elementos. El aire tiene oxígeno (O) y nitrógeno (N). Las plantas, personas y todos los seres vivos tienen una gran cantidad de carbono (C). Jueguen con la simulación hasta descubrir qué partícula (o partículas) determina el nombre del elemento que construyeron. ¿Qué descubriste?
6) Jueguen con la simulación hasta descubrir qué partículas afectan la masa del átomo o ion. ¿Cuáles partículas son pesadas y cuáles son ligeras?
Por último, ¡pongan a prueba su aprendizaje con juegos! Resuelvan los niveles 1 y 2 del MODO JUEGO de la simulación. Si se animan también pueden probar los niveles 3 y 4.
10. Autoevaluación
Para seguir pensando y practicando los conceptos que vimos en este bloque, te proponemos realizar la siguiente actividad de auto-evaluación, a la que pueden acceder haciendo clic en Cuestionario.
|
Si no tenés un usuario creado en este campus no podés hacer las autoevaluaciones. Te dejamos las instrucciones para poder realizarlas:
|