Uniones químicas y propiedades de las sustancias
| Sitio: | Campus Claves Académica |
| Curso: | Química - EnlaceUBA |
| Libro: | Uniones químicas y propiedades de las sustancias |
| Imprimido por: | Invitado |
| Día: | jueves, 11 de junio de 2026, 08:18 |
Tabla de contenidos
- 1. Introducción a los enlaces químicos
- 2. Regla del octeto
- 3. Tres tipos de uniones químicas
- 4. ¿De qué depende el tipo de unión que ocurre entre los átomos?
- 5. ¿Cuál es la relación entre la estructura química y las propiedades que presentan las sustancias?
- 6. ¿De qué depende el punto de fusión y ebullición de las sustancias?
- 7. Propiedades de los sólidos iónicos
- 8. Propiedades de las sustancias Moleculares
- 9. Propiedades de los metales
- 10. Autoevaluación
- 11. Tu opinión es clave
1. Introducción a los enlaces químicos
La mayoría de los elementos no se encuentran libres en la naturaleza sino formando parte de diferentes compuestos. Los elementos sodio y cloro, por ejemplo, están presentes en el cloruro de sodio, la sal común, NaCl. El carbono forma parte de sustancias muy conocidas, por ejemplo, dióxido de carbono, CO2 (que producimos al respirar, que utilizan las plantas en el proceso de fotosíntesis); del etanol, C2H5OH (alcohol de las bebidas, el mismo que hay en los botiquines de primeros auxilios, que se produce durante la fermentación de la glucosa de las frutas para obtener vino o sidra); de la sacarosa, azúcar de mesa, C12H22O11; del metano, CH4, componente del gas natural; entre muchísimos otros compuestos, y también se encuentra naturalmente como sustancia simple en el diamante y el grafito (mina de lápiz). Algunas preguntas que intentaremos responder durante el recorrido de este bloque son: ¿Cómo los elementos se combinan unos con otros? ¿Qué fuerzas mantienen unidos a los átomos, iguales o diferentes, en una molécula? ¿Todas las sustancias están formadas por moléculas? ¿Qué propiedades tienen estas sustancias?
Las propiedades de las sustancias dependen en gran medida de la naturaleza de los enlaces que unen sus átomos. Existen tres tipos principales de enlaces químicos que vamos a estudiar en este bloque: enlace iónico, enlace covalente y enlace metálico. Estos enlaces, al condicionar las propiedades de las sustancias que los presentan, permiten clasificarlas en: sustancias iónicas (llamadas comúnmente SALES), covalentes (conocidas como sustancias moleculares y llamadas comúnmente MOLÉCULAS) y sustancias metálicas (llamadas METALES).
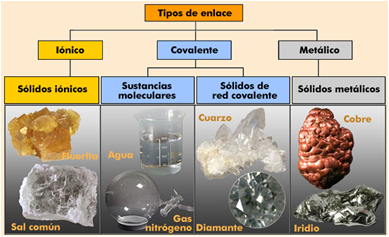
El desarrollo de la tabla periódica actual y la determinación de las configuraciones electrónicas dieron a los químicos los fundamentos para poder entender cómo se forman las sustancias (simples o compuestas, moleculares o iónicas). Recordemos que los elementos pertenecientes a un mismo grupo de la tabla periódica tienen generalmente propiedades químicas similares y sus átomos, la misma configuración electrónica externa (CEE). Esto quiere decir que presentan el mismo número de electrones en su orbital más externo (el más alejado al núcleo del átomo). Existe una estrecha relación entre el número de electrones externos y el comportamiento químico de los átomos; en particular, si se consideran los elementos representativos (grupos 1, 2 y del 13 al 18). Los electrones más externos son muy importantes ya que son los que intervienen en los enlaces químicos y se denominan electrones de valencia. Conocer el número de electrones de valencia nos ayuda a predecir de qué manera se unirá ese átomo con otro. Para los elementos representativos de la tabla Periódica, el número de grupo (en la Tabla Periódica) coincide con su número de electrones de valencia, como pueden ver en la siguiente Tabla:
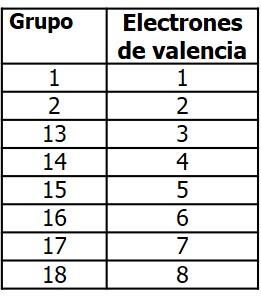
2. Regla del octeto
Según la regla del octeto los átomos pueden ceder electrones, aceptar electrones o compartir electrones para enlazarse con otros átomos y así adquirir la Configuración Electrónica Externa (CEE) del gas noble más próximo en la tabla periódica, y de esa manera completar con 8 electrones su orbital más externo.
¿Por qué los átomos quieren adquirir la CEE del gas noble más próximo en la Tabla Periódica (o más cercano en número atómico)? Porque los gases nobles son sustancias extraordinariamente poco reactivas. Todos ellos son monoatómicos, lo que significa que no tienen tendencia a combinarse con ningún átomo, ni siquiera con ellos mismos. Se escasa reactividad llevo a pensar que su configuración electrónica es más estable que la de otros elementos. Hoy sabemos que los átomos tienden a combinarse de manera de adquirir una configuración electrónica que les otorgue la mayor estabilidad posible. Por eso tienden a combinarse de manera de adquirir la CEE del gas noble más cercano en número atómico.
¿Por qué se unen los átomos? Lo hacen para llegar al estado de mínima energía (más estable), es decir que, cuando dos átomos se unen para formar un enlace estable se libera cierta cantidad de energía. Esa misma energía debemos entregar si queremos romper la unión química.
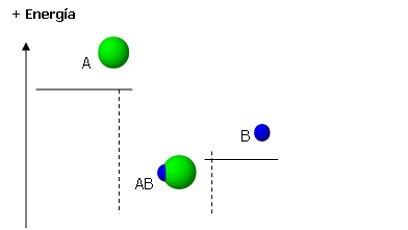
El gráfico representa la energía que presentan un átomo A y un átomo B en forma aislada en estado inicial, y la energía del compuesto AB cuando éstos átomos se enlazan por medio de una unión química. Noten que la energía del compuesto AB es menor que la energía de los átomos A y B.
3. Tres tipos de uniones químicas
Veamos con mayor detalle los tres tipos de uniones químicas que vamos a aprender en esta unidad:
- Uniones Metálicas, que ocurren entre los metales
- Uniones Covalentes, que permiten la formación de moléculas
- Uniones Iónicas, que permiten la formación de compuestos iónicos que llamamos comúnmente sales.
Los átomos de los elementos metálicos, cuando no forman parte de sales u óxidos, se mantienen juntos a través de lo que llamamos uniones METÁLICAS. Los átomos de los metales tienen pocos electrones en su última capa, por lo general 1, 2 ó 3. Éstos átomos pierden fácilmente esos electrones (electrones de valencia) y se convierten en iones positivos, por ejemplo Na+, Ag+, Cu2+, Mg2+. Los iones positivos resultantes (cationes) se ordenan en el espacio formando la red metálica. Los electrones de valencia desprendidos de los átomos metálicos forman una nube de electrones que puede desplazarse a través de toda la red. En el siguiente esquema se muestra el conjunto de los iones positivos metálicos en el metal plata (Ag+), unidos mediante una nube de electrones deslocalizados (simbolizados como puntos de color azul), con carga negativa, que los envuelve:
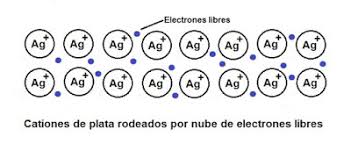
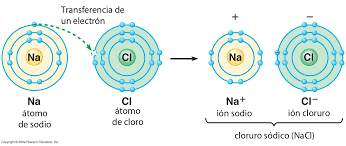
Los átomos de los elementos metálicos, además de formar uniones metálicas, también pueden formar uniones con los átomos no metálicos. Acá el acuerdo es sencillo: los metales fácilmente ceden sus electrones y los no metales no tienen ningún problema en aceptarlos. De esta manera, los átomos metálicos forman iones positivos (cationes) y los no metálicos iones negativos (aniones), que quedan unidos porque sus cargas son contrarias y SE ATRAEN FUERTEMENTE. Estas uniones se llaman IÓNICAS. En la figura de abajo se muestra como un átomo de Sodio (Na; metal) cede un electrón a un átomo de Cloro (Cl; no metal), quedando el Na con carga neta positiva (catión) unido al Cloro con carga neta negativa (anión) por medio de un enlace iónico:
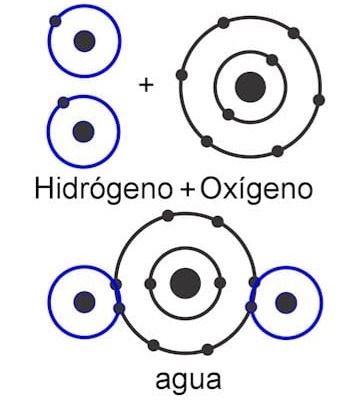
Los átomos de los elementos no metálicos llegan a completar el octeto compartiendo electrones entre ellos. Ninguno quiere perder sus electrones de valencia, pero necesitan los electrones de otros átomos para llegar a completar con 8 electrones su orbital más externo; entonces, comparten electrones. Estas uniones en las que los átomos comparten electrones se llaman COVALENTES y dan lugar a la formación de MOLÉCULAS. Moléculas como el agua (H2O), el oxígeno (O2) o el dióxido de carbono (CO2). En la figura de abajo se muestran los enlaces covalentes entre 2 átomos de Hidrógeno (H) y 1 átomo de Oxígeno (O) en la molécula de agua (H2O):
En resumen:
- en las uniones COVALENTES, los átomos implicados en el enlace COMPARTEN ELECTRONES, y este tipo de unión ocurre entre ELEMENTOS NO METÁLICOS;
- en las uniones IÓNICAS, existe una TRANSFERENCIA DE ELECTRONES de un átomo al otro, de manera que el ELEMENTO METÁLICO forma un catión (ion de carga positiva) y el ELEMENTO NO METÁLICO forma un anión (ion de carga negativa), y CATIONES Y ANIONES quedan unidos por la atracción de sus cargas contrarias;
- en las uniones METÁLICAS, participan elementos de carácter METÁLICO, que ceden fácilmente electrones y así los elementos metálicos quedan unidos por esta ¨red¨ de electrones que circulan libremente entre ellos.
Ya sea porque los átomos involucrados comparten electrones o porque ganan o pierden electrones, el "objetivo" es tener la capa electrónica más externa completa (como los gases nobles) y a esta regla, como vimos antes, la llamamos regla del octeto.
4. ¿De qué depende el tipo de unión que ocurre entre los átomos?
Para entender de qué depende que los átomos se enlacen por medio de uniones iónicas o covalentes, repasemos dos propiedades de los átomos que vimos en el bloque llamado ¨Clasificación Periódica¨: la electronegatividad y la energía de ionización.
Existen átomos como los no metales (especialmente el nitrógeno, el oxígeno y los halógenos (elementos del grupo 17: F, Cl, Br, I) que tienen una tendencia fuerte a atraer electrones ya que presentan altos valores de electronegatividad y alta energía de ionización. Fíjense que a todos ellos les faltan pocos electrones para completar el octeto (tienen 7 electrones en su orbital más externo y sólo les falta 1 electrón para completar el octeto). En cambio, los metales alcalinos y alcalinos térreos presentan bajas electronegatividades y baja energía de ionización, por lo tanto tienen tendencia a perder electrones fácilmente. Si estos elementos pierden los pocos electrones de valencia que tienen (1 ó 2) alcanzan la configuración del gas noble más cercano y quedan con la capa completa (con 8 electrones en su último orbital).
Teniendo en cuenta esto, ¿por qué algunos átomos forman enlaces covalentes y otros forman enlaces iónicos o metálicos?
Veamos. Si dos elementos tienen baja tendencia a perder sus electrones (alta energía de ionización) y tienen tendencias parecidas a atraer electrones (electronegatividades similares) van a compartir electrones y formar enlaces covalentes. Ninguno de los átomos va a querer perder sus electrones pero están interesados en completar el octeto: mejor compartir. Estos elementos por lo general son no metales. Por lo tanto, los no metales tienden a formar enlaces covalentes entre ellos.
En cambio, si tenemos un elemento con mucha tendencia a formar cationes (baja energía de ionización) como un metal alcalino y otro que tiende a atraer electrones (alta electronegatividad) como un no metal, seguramente ocurra una transferencia de electrones: el metal alcalino le cede sus electrones al no metal. El metal forma un catión y el no metal un anión, que se atraen fuertemente entre sí porque sus cargas eléctricas son contrarias. El enlace que se forma entonces es un enlace iónico. Los metales tienden a formar enlaces iónicos con los no metales.
Si tenemos muchos átomos metálicos, como en una pieza de metal, todos van a tener una tendencia considerable a perder sus electrones y formar cationes (energías de ionización bajas). Forman entonces lo que llamamos un enlace metálico. Los átomos que forman una pieza de metal están en la forma de cationes. Sus electrones de valencia están débilmente unidos y no están asociados a ningún átomo metálico en particular. Recuerden que los metales tienen baja tendencia a atraer electrones en un enlace (tienen baja electronegatividad). Son compartidos por toda la pieza de metal, por todo el "cristal metálico".
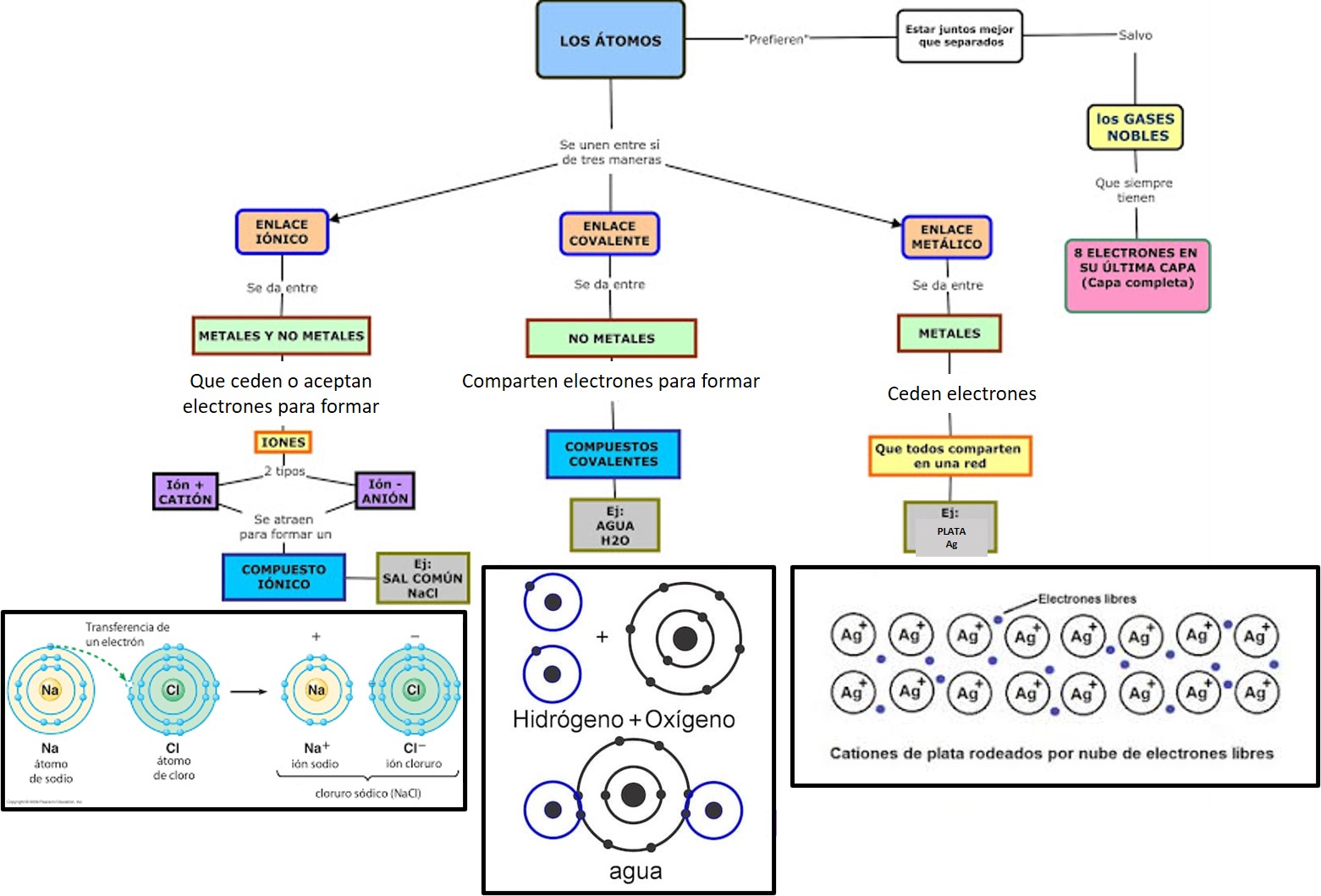
En el siguiente cuadro sinóptico se sintetizan las principales características de estos tres tipos de enlaces químicos:
5. ¿Cuál es la relación entre la estructura química y las propiedades que presentan las sustancias?
Hasta aquí aprendimos que existen 3 tipos principales de uniones químicas entre los átomos que dan lugar a todas las sustancias y cosas que conocemos: UNIONES IÓNICAS que forman SALES, UNIONES COVALENTES que ocurren en las moléculas y UNIONES METÁLICAS presentes entre los metales. Como dijimos anteriormente, para poder interpretar y/o predecir las propiedades de las diferentes sustancias, debemos conocer a qué tipo pertenecen. En adelante vamos a examinar la relación entre la estructura química y las propiedades que presentan las sustancias.
Habitualmente usamos sustancias que tienen propiedades muy diferentes. A temperatura ambiente, la sal, el azúcar y el cobre son sólidos, el agua y el alcohol son líquidos, el oxígeno, el dióxido de carbono, el metano y el amoníaco son gases.
Si bien la sal y el azúcar comparten algunas propiedades -como ser sólidos cristalinos, blancos y solubles en agua-, no comparten otras, como la temperatura a la cual funden. Si calentamos suavemente azúcar en una cacerola, funde fácilmente, obteniéndose el conocido “caramelo”. En cambio, no podemos transformar la sal sólida en sal líquida con el calor que genera el fuego de la hornalla, porque la temperatura de fusión del NaCl es mucho mayor que la temperatura de fusión de la sacarosa, nombre químico del azúcar común, C12H22O11 y que la que se alcanza con la llama de la hornalla. Por otra parte, estas sustancias casi no comparten propiedades con el cobre, más allá de ser sólidas a temperatura ambiente.
El oxígeno, el amoníaco, el metano y el dióxido de carbono son sustancias gaseosas a temperatura ambiente; pero sus propiedades son bien distintas. El olor picante y desagradable del amoníaco, NH3, es muy característico; en cambio, el oxígeno, O2, no tiene olor. El metano, CH4, es un combustible, mientras que el dióxido de carbono, CO2, es un producto de la combustión. El oxígeno favorece la combustión mientras que el CO2 se utiliza para lo contrario, en los extintores contra incendios (matafuegos).
¿Dónde radica la causa de las semejanzas y las diferencias en el aspecto y comportamiento de las distintas sustancias? Comencemos por analizar qué ocurre durante los cambios de estado:
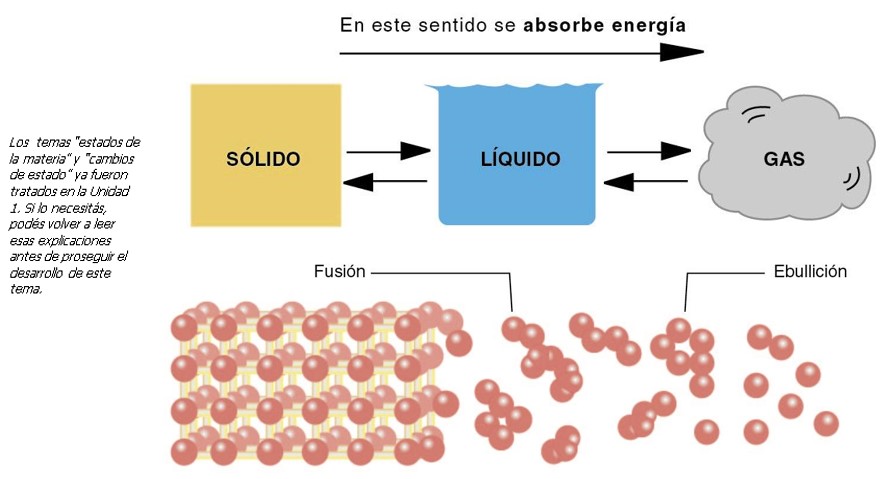
Para que se produzca el pasaje de una sustancia del estado sólido al estado líquido (recordà que dicho cambio se denomina fusión), es necesario entregar energía (generalmente en forma de calor) a dicha sustancia para “vencer” las fuerzas de atracción que mantienen a sus partículas vibrando alrededor de determinadas posiciones (estado sólido), y que así puedan deslizarse unas sobre otras (estado líquido).
Algo similar sucede durante la vaporización: debemos entregar energía suficiente para que las partículas de un líquido logren separarse disminuyendo, entonces, la intensidad de las fuerzas de atracción entre ellas. Cuanto más intensas sean las interacciones que hay entre las partículas, mayor cantidad de energía será necesaria para separarlas y, por lo tanto, mayor será la temperatura a la que ocurre el cambio de estado.
Por lo tanto, el estado de agregación de una sustancia a una temperatura dada depende de la intensidad de las fuerzas que hay entre las partículas que lo forman.
Las SUSTANCIAS IÓNICAS O SALES forman CRISTALES como los que se ven en la imagen de abajo, donde se alternan CATIONES y ANIONES en la estructura, unidos por fuerzas eléctricas intensas entre las cargas positivas y negativas. La fórmula química indica la proporción de los componentes del cristal. Por ejemplo, un cristal de cloruro de sodio tiene la siguiente fórmula química: NaCl, que indica que por cada catión Na+ hay un anión Cl-. Las fuerzas que mantienen la estructura de cristal son las fuerzas de la unión iónica. Las sales son SÓLIDAS a temperatura ambiente:

Las SUSTANCIAS METÁLICAS o METALES también formaban cristales como se ve en esta otra imagen, por eso la mayoría de los metales son SÓLIDOS a temperatura ambiente, a excepción del Hg (mercurio):

Ahora bien, las sustancias en las que los átomos se enlazan por UNIONES COVALENTES forman MOLÉCULAS. En este caso, la fórmula química indica cómo está compuesta la molécula. Por ejemplo, el gas Cl2 está formado por unidades de Cl-Cl, es decir, moléculas en las que hay dos cloros unidos por un enlace covalente simple. Las sustancias como el gas Cl2, el dióxido de carbono (CO2), el agua (H2O), el metano (CH4), el etanol (C2H6O) o el azúcar de mesa (C12H22O11) están formadas por moléculas. En cada molécula, los átomos se mantienen unidos por enlaces covalentes y a su vez las moléculas se encuentran unidas entre sí por otras fuerzas, que llamamos fuerzas intermoleculares (ENTRE moléculas). Estas fuerzas son muy débiles en el gas Cl2 o en el CO2, por lo que estas sustancias se encuentran en forma de gases a temperatura ambiente. En el agua, el etanol o el azúcar de mesa, las fuerzas intermoleculares son más intensas y por lo tanto, las moléculas logran mantenerse unidas formando un líquido en el caso del agua y el etanol, y un sólido en el caso del azúcar a temperatura ambiente. Como ven el estado de agregación (sólido, líquido o gaseoso) en las sustancias moleculares depende fundamentalmente de la INTENSIDAD O MAGNITUD de las fuerzas entre sus moléculas. La magnitud de estas fuerzas a su vez depende de la geometría (distribución de los átomos de la molécula en el espacio), tamaño de la molécula y distribución de sus cargas. En la imagen de abajo se muestra en forma esquemática la geometría de distintas moléculas:
6. ¿De qué depende el punto de fusión y ebullición de las sustancias?
Principalmente, del tipo de partículas que forman esas sustancias y de las fuerzas de atracción entre esas partículas.
En el siguiente cuadro te mostramos algunos ejemplos: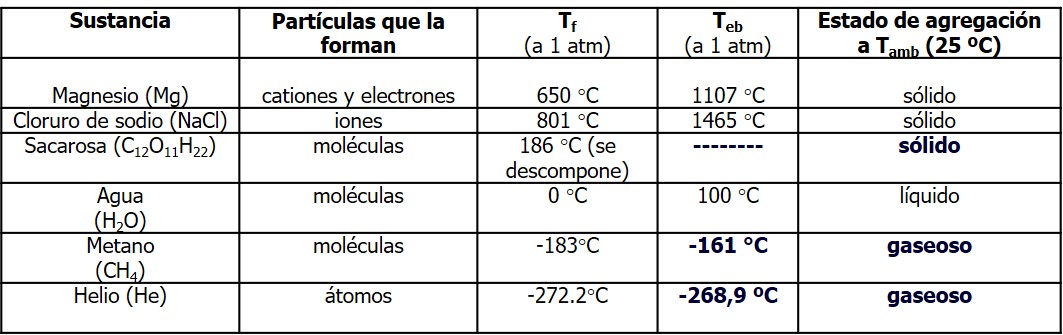
Estados de agregación a temperatura ambiente:
En general, de acuerdo con el tipo de enlace, hay regularidades en el estado de agregación de las distintas sustancias a temperatura ambiente:
- Metales: sólidos (a excepción del mercurio) a temperatura ambiente y poseen puntos de fusión relativamente altos.
- Sustancias iónicas: sólidas a temperatura ambiente y, en general, tienen muy altos puntos de fusión, como la sal, NaCl.
- Sustancias moleculares: sólidos (de alto o bajo punto de fusión), líquidos o gases a temperatura ambiente.
Las fuerzas de atracción entre las partículas se deben a interacciones eléctricas y su intensidad depende del tipo de partículas que interactúen. En el caso de los metales, la interacción se da entre los cationes metálicos y los electrones que circulan entre ellos. En los compuestos iónicos, la interacción se da entre cationes y aniones por la atracción electrostática de cargas de diferente signo. Estas fuerzas entre iones de diferente carga son mucho más intensas que las que pueden producirse entre moléculas. Por este motivo, el punto de fusión de las sustancias iónicas es siempre muy alto, lo que no ocurre con las sustancias moleculares.
Para el caso de sustancias moleculares, es preciso que no confundas las uniones intramoleculares (uniones covalentes, entre los átomos que forman la molécula) con las intermoleculares (que son interacciones que ocurren entre las moléculas). No vamos a profundizar en las uniones que existen entre las moléculas pero sí queremos que sepas que existen y condicionan el punto de fusión y ebullición de las moléculas.
En conclusión, conocer la estructura de las sustancias nos ayuda a entender sus propiedades físicas y químicas, y viceversa. En el siguiente cuadro se resumen las características generales de las distintas sustancias:
|
|
Sustancias metálicas |
Sustancias iónicas |
Sustancias covalentes |
|
Estado de agregación a temp. ambiente |
Sólido (excepción es el Hg), tienen alto punto de fusión. |
Sólidos de muy alto punto de fusión. |
Sólidos, líquidos o gases. Presentan bajo punto de fusión. |
|
Conducción de corriente eléctrica |
En estado sólido y líquido: sí. |
En est. sól: no. En est. líq: sí. |
En estado sól y líq: no. |
7. Propiedades de los sólidos iónicos
Los sólidos iónicos están formados por iones unidos por fuerzas eléctricas intensas (enlaces iónicos) entre iones contiguos con cargas opuestas (cationes y aniones). En estas sustancias no hay moléculas sencillas e individuales; en cambio, los iones permanecen en una ordenación repetitiva y regular formando una red continua.
En la sal común los iones Na+ (cationes) y los iones Cl- (aniones), unidos por fuerzas eléctricas debidas a su carga opuesta, forman una red tridimensional cúbica en la que cada ion Cl- está rodeado por seis iones Na+ y cada ion Na+ por seis iones Cl-.
Debido a su estructura, los sólidos iónicos tienen las siguientes propiedades:
1. No son volátiles y tienen un punto de fusión alto (normalmente entre 600 °C y 2000 °C). Para fundir el sólido deben romperse los enlaces iónicos, separando unos de otros los iones con cargas opuestas. Los iones adquieren energía cinética suficiente para que esto ocurra solamente a temperaturas elevadas.
2. Los sólidos iónicos no conducen la electricidad, puesto que los iones cargados tienen posiciones fijas. Sin embargo, llegan a ser buenos conductores cuando están fundidos o disueltos en agua. En ambos casos, fundidos o en disolución, los iones son libres para moverse a través del líquido y así pueden conducir una corriente eléctrica.
3. Muchos compuestos iónicos, pero no todos (p. ej., el NaCl pero no el CaCO3), son solubles en agua.
8. Propiedades de las sustancias Moleculares
Prácticamente todas las sustancias que son gases o líquidos a 25 ºC y a la presión normal son moléculas. Estas sustancias están constituidas por partículas discretas llamadas moléculas, que a su vez están formadas por dos o más átomos unidos por unas fuerzas muy intensas llamadas enlaces covalentes. En cambio las fuerzas ENTRE las moléculas próximas son bastante débiles.
Algunos ejemplos de sustancias moleculares que son líquidos en condiciones normales son: el agua (H2O) y el alcohol etílico (C2H6O2); y ejemplos de sustancias moleculares que son gases en condiciones normales son: el nitrógeno del aire (N2) o el dióxido de carbono (CO2).
Para fundir o hacer hervir una sustancia molecular, las moléculas deben separarse unas de otras. La debilidad de las fuerzas de atracción entre las moléculas que componen estas sustancias hace que se necesite poca energía para separarlas por lo que presentan bajos puntos de fusión y de ebullición. En cambio, en estas transformaciones los enlaces covalentes dentro de las moléculas permanecen intactos.
También existen sustancias moleculares sólidas a temperatura ambiente. Los átomos que forman estas sustancias están unidos por una red continua de enlaces covalentes, formando lo que se denomina una red cristalina. Entre las sustancias que forman sólidos de red covalente se encuentran tanto elementos, por ejemplo el diamante (C), como compuestos, por ejemplo el cuarzo (SiO2).
En el diamante los enlaces covalentes C -C se extienden a través del cristal formando una estructura tridimensional tetraédrica.
En el cuarzo, cada átomo de silicio se une tetraédricamente a cuatro átomos de oxígeno. Cada átomo de oxígeno se une a dos silicios y así une tetraedros contiguos entre sí. Esta red de enlaces covalentes se extiende a través de todo el cristal.
Los sólidos de red covalente presentan propiedades características:
- Son muy duros.
- Tienen elevado punto de fusión, con frecuencia alrededor de 1.000 °C o mayores. Esto es debido a que para fundir el sólido, deben romperse los fuertes enlaces covalentes entre sus átomos.
- Son insolubles en todos los disolventes comunes. Para que se disuelvan, tienen que romperse los enlaces covalentes de todo el sólido.
- Son malos conductores de la electricidad. En la mayoría de las sustancias de red covalente no hay electrones móviles que puedan transportar una corriente.
9. Propiedades de los metales
Los cristales metálicos están formados por un conjunto ordenado de iones positivos, por ejemplo, Na+, Mg2+, Cu2+. Estos iones están anclados en su posición, como boyas en un "mar" móvil de electrones. Estos electrones no están sujetos a ningún ion positivo concreto, sino que pueden deambular a través del cristal. Esta estructura explica muchas de las propiedades características de los metales:
1. Conductividad eléctrica elevada. La presencia de un gran número de electrones móviles explica por qué los metales tienen conductividades eléctricas varios cientos de veces mayores que los no metales. La plata es el mejor conductor eléctrico pero es demasiado caro para uso normal. El cobre, con una conductividad cercana a la de la plata, es el metal utilizado habitualmente para cables eléctricos.
2. Buenos conductores del calor. El calor se transporta a través de los metales por las colisiones entre electrones, que se producen con mucha frecuencia.
3. Ductilidad y maleabilidad. La mayoría de los metales son dúctiles (capaces de ser estirados para obtener cables) y maleables (capaces de ser trabajados con martillos en láminas delgadas). En un metal, los electrones actúan como un pegamento flexible que mantiene los núcleos atómicos juntos, los cuales pueden desplazarse unos sobre otros. Como consecuencia de ello, los cristales metálicos se pueden deformar sin romperse.
4. Insolubilidad en agua y en otros disolventes comunes. Ningún metal se disuelve en agua; los electrones no pueden pasar a la disolución y los cationes no pueden disolverse por ellos mismos.
10. Autoevaluación
Para seguir pensando y practicando los conceptos que vimos en este bloque, te proponemos realizar la siguiente actividad de auto-evaluación, a la que pueden acceder haciendo clic en Cuestionario
|
Si no tenés un usuario creado en este campus no podés hacer las autoevaluaciones. Te dejamos las instrucciones para poder realizarlas:
|