Soluciones
| Sitio: | Campus Claves Académica |
| Curso: | Química - EnlaceUBA |
| Libro: | Soluciones |
| Imprimido por: | Invitado |
| Día: | domingo, 17 de mayo de 2026, 08:16 |
Tabla de contenidos
- 1. ¿Qué son las soluciones?
- 2. ¿Por qué algunas sustancias son solubles en determinados solventes y otras no? ¿De qué depende la solubilidad?
- 3. Solubilidad
- 4. Soluciones Saturadas versus Soluciones no saturadas
- 5. Distintas formas de expresar la concentración de las soluciones
- 6. Ejemplos
- 7. Resolución de problemas: cuando el soluto está en estado líquido y el solvente es un líquido también
- 8. Más ejemplos... Cuando el soluto está en estado sólido y el solvente está en estado líquido
- 9. ¡Disolver y diluir NO son lo mismo!
- 10. Ejemplos de diluciones
- 11. Autoevaluación
- 12. Unos minutos y ya te vas
1. ¿Qué son las soluciones?
Las soluciones son mezclas homogéneas (es decir que presentan 1 única fase) cuyas propiedades intensivas se mantienen constantes en todo el sistema. Las mezclas son sistemas cuya composición es variable. No es posible escribir una fórmula química para representar una mezcla, porque una mezcla posee varios componentes (al menos dos). Las soluciones son mezclas compuestas por un soluto (o varios) y un solvente. Uno de los criterios que se utiliza para definir cuál de los componentes de la mezcla es el soluto y cuál es el solvente es designar al solvente como el componente que se encuentra en cantidad predominante, siendo el otro el soluto. El agua SIEMPRE se considera solvente, aún cuando está en menor proporción. Por ejemplo, en una solución acuosa que tiene 98% de etanol, el agua será el solvente y el alcohol el soluto.
Veamos esto con un ejemplo de un solvente líquido y un soluto sólido:

Si nos imaginamos cómo se vería a nivel de las partículas, sería algo así:
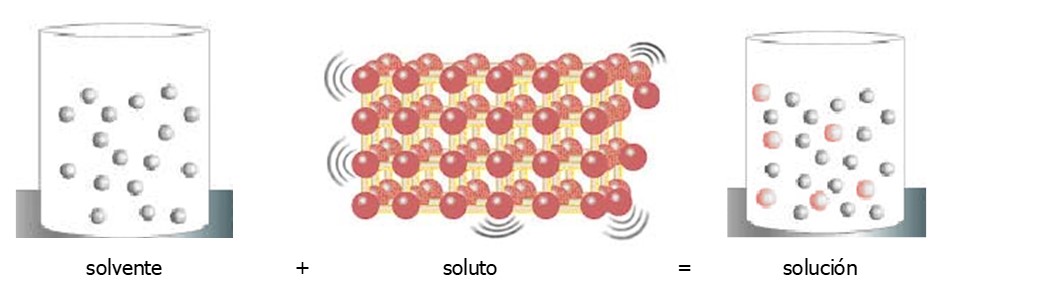
En esta Tabla se indican distintos tipos de soluciones que pueden existir:
|
Soluto |
Solvente |
Estado de la solución resultante |
Ejemplos |
|
Gas |
Gas |
Gas |
Aire |
|
Gas |
Líquido |
Líquido |
Soda (CO2 disuelto en agua) |
|
Gas |
Sólido |
Sólido |
H2 gaseoso en paladio |
|
Líquido |
Líquido |
Líquido |
Alcohol en agua |
|
Sólido |
Líquido |
Líquido |
Sal en agua |
|
Sólido |
Sólido |
Sólido |
Aleaciones: bronce. |
Como pueden apreciar en la Tabla, el estado físico (sólido, líquido, gaseoso) de la MEZCLA del soluto y el solvente (lo que llamamos SOLUCIÓN o solución resultante en la Tabla) siempre coincide con el estado físico del SOLVENTE; es decir, si el solvente es líquido, la solución será líquida o si el solvente es gaseoso, la solución estará en estado gaseoso.
2. ¿Por qué algunas sustancias son solubles en determinados solventes y otras no? ¿De qué depende la solubilidad?
Para que un soluto se disuelva en un solvente, primero deben vencerse las fuerzas de atracción entre las partículas (átomos, moléculas o iones) que lo forman y separarlas de manera que las partículas de solvente sean capaces de intercalarse entre las de soluto. Por ejemplo, si disolvemos azúcar en agua, tendremos la disolución de un soluto sólido en un solvente formado por moléculas en agua.
A grandes rasgos, podemos imaginar la disolución como un proceso en tres etapas: i- en la primera etapa se separan las moléculas de soluto (azúcar); ii- en la segunda se separan las moléculas de solvente (en esta etapa se necesita gastar energía para vencer las fuerzas de atracción entre las partículas se solvente); iii- se mezclan las moléculas de solvente y las de soluto. En algunos casos estos procesos ocurren en forma espontánea, en otros no. Además, estos procesos pueden ser endotérmicos (quiere decir que se necesita energía en forma de calor para que ocurran, por ejemplo, se necesita calentar la mezcla) o exotérmicos (se libera energía en forma de calor cuando ocurre la mezcla).
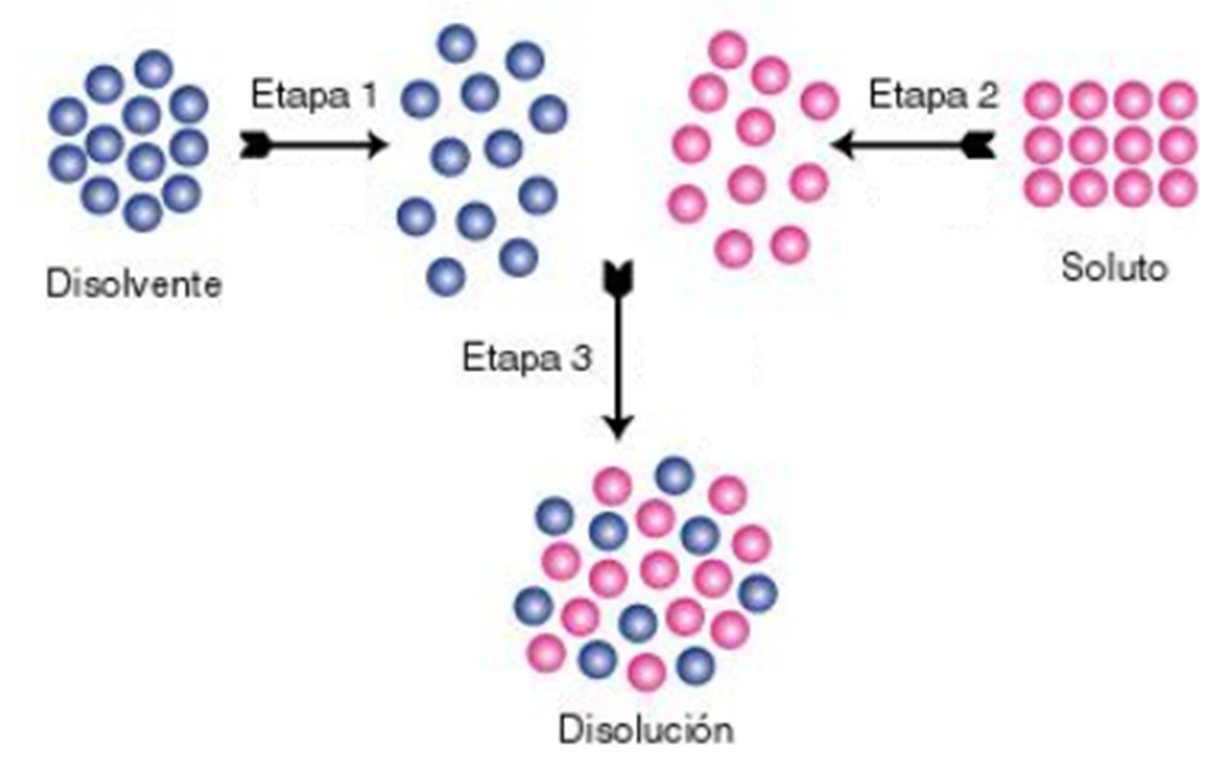
3. Solubilidad
Se denomina solubilidad a la concentración de la solución saturada a una presión y temperatura dada. La solubilidad se expresa generalmente como gramos (g) de soluto/100g de solvente o g de soluto/100 ml de solvente.
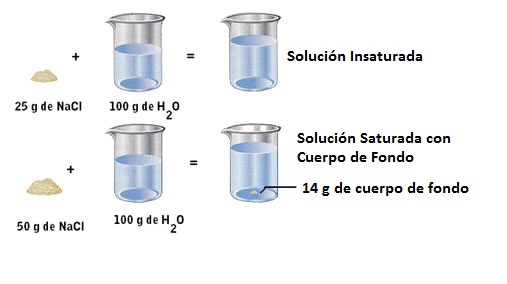
La solubilidad de los sólidos en los líquidos siempre es limitada y depende de la naturaleza del soluto, del solvente, de la temperatura principalmente y muy poco de la presión. Esto quiere decir, por ejemplo, que si estamos disolviendo sal de mesa (NaCl) en agua (como se muestra en la figura de abajo), no podemos agregar sal (soluto) indefinidamente al agua (solvente). En el primer ejemplo se agregan 25 g de sal a 100 mL de agua, y se obtiene una solución NO SATURADA o INSATURADA (donde todo el soluto se disuelve en el solvente). Sin embargo, si seguimos agregando sal, en un punto, cuando lleguemos al límite de saturación, esa dada cantidad de agua (solvente) ya no podrá disolver la sal y se formará un precipitado en el fondo del vaso (es decir que quedara la sal en forma sólida en el fondo del vaso). Esto es lo que ocurre en el segundo caso que muestra la imagen de abajo: al tratar de disolver 50 g de sal en 100 mL de agua se obtiene una solución SATURADA; en esta solución 36 g de sal se disuelven y 14 g de sal no se disuelven y quedan en el fondo del vaso en forma de precipitado.
Como dijimos antes, en el caso de la solubilidad de los sólidos en los líquidos, la Temperatura es condicionante de dicha solubilidad, pero no tanto la Presión.
En cambio, si estamos considerando la solubilidad de los gases en líquidos tanto la presión como la temperatura deben tenerse en cuenta: en este caso la solubilidad aumenta con la presión y disminuye con la temperatura. ¿Qué ejemplos de la vida cotidiana se les ocurren? Piensen qué ocurre con el gas al destapar una botella de gaseosa o al hervir agua...
4. Soluciones Saturadas versus Soluciones no saturadas
Como mencionamos previamente, existe una cantidad máxima de soluto sólido que se puede disolver en un determinado volumen de solvente líquido a una determinada temperatura antes de que el sistema se transforme en heterogéneo. A esto se llama límite de saturación. Teniendo en cuenta el límite de saturación, las soluciones se pueden clasificar en SOLUCIONES SATURADAS Y NO SATURADAS.
Las SOLUCIONES SATURADAS son aquellas que presentan una cantidad mayor a la máxima cantidad de soluto que puede disolverse en un determinado volumen de solvente a una dada temperatura, es decir que alcanzaron o superaron el límite de saturación. El límite de saturación es la máxima cantidad de soluto que puedo disolver en un determinado volumen de solvente a una cierta temperatura y presión.
Pensemos en la siguiente situación: si tratamos de disolver azúcar en un vaso de agua (que tiene 200 mL de agua), ¿podremos agregar azúcar indefinidamente, mezclar y siempre observar que el azúcar se disuelve? No, esos 200 ml de agua son capaces de disolver una cierta cantidad de azúcar, pero el exceso de soluto que no pudo disolverse va a precipitar. Entonces el sistema se transformará en heterogéneo, porque al precipitar el exceso de soluto en las soluciones saturadas se observan dos fases: el soluto precipitado en el fondo y la solución saturada de azúcar y agua por encima. Las soluciones saturadas están en un equilibrio dinámico con un exceso de soluto sin disolver. En el equilibrio dinámico, las velocidades de precipitación y de disolución del soluto son iguales, como se muestra en la imagen de abajo. Poniéndonos un poco más técnicos: se denomina solución saturada a aquella que está o puede estar en equilibrio dinámico con un exceso del soluto sin disolver.
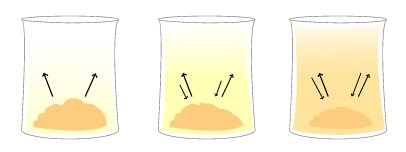
- Al colocar un soluto en agua comienza a disolverse;
- La velocidad de disolución es mayor que la de precipitación (observá el tamaño de las flechas);
- Se llega a un equilibrio dinámico: las velocidades de disolución y precipitación son iguales.
En cambio en las SOLUCIONES NO SATURADAS, la cantidad de soluto disuelto es menor al límite de saturación, esto quiere decir, que es menor a la máxima cantidad de soluto que admite esa cantidad de solvente.
Se suele utilizar una distinción entre soluciones diluidas (donde la cantidad de soluto disuelto es mucho menor que el límite de saturación) y soluciones concentradas (donde la cantidad de soluto disuelto es cercana al límite de saturación), pero esta última clasificación es un tanto grosera y es sólo cualitativa. Con esto queremos decir que puede ser útil para comparar soluciones y establecer cuándo una solución es más o menos concentrada que otra, pero no nos da información para identificar inequívocamente una solución particular. Por ejemplo, como se ve en la figura de abajo las dos soluciones del medio no se pueden identificar inequívocamente:
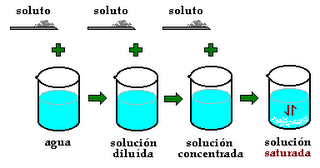
Siempre que tengamos un sistema heterogéneo, como en el caso de la solución saturada, y no haya disminución de la cantidad de soluto en el fondo (o aumento en la intensidad del color de la solución) con el tiempo, podemos afirmar que la solución que se observa sobre el residuo sólido del fondo está saturada.
Si tenemos un sistema homogéneo, es decir que no hay exceso de soluto en el fondo, sólo podemos comprobar que la solución está saturada agregando una pequeñísima cantidad de soluto y viendo si se disuelve (con lo cual sería no saturada) o si no se disuelve y precipita en el fondo (ya estaría saturada, porque no admite más soluto en solución). La otra manera es preparar la solución con los datos de las tablas de solubilidad y disolver exactamente la cantidad de soluto necesaria para la saturación.
A MODO DE RESUMEN...
- Se denomina solubilidad a la concentración de la solución saturada a una presión y temperatura dada.
- La solubilidad se expresa generalmente, en g de soluto/100g de solvente ó g de soluto/100 ml de solvente.
- La solubilidad varía con la temperatura y la presión.
- La solubilidad de los sólidos en los líquidos es siempre limitada y depende de la naturaleza del solvente, de la del soluto, de la temperatura y muy poco de la presión.
- La presión tiene una gran importancia cuando se consideran solubilidades de gases.
- La solubilidad de los gases aumenta al disminuir la temperatura.
- La solubilidad de los gases aumenta al aumentar la presión.
5. Distintas formas de expresar la concentración de las soluciones
Imaginemos 3 soluciones de dicromato de potasio (sal naranja) en agua, como las que se observan en la siguiente imagen:

¿Cómo podríamos diferenciarlas entre sí? ¿Cómo diferenciamos soluciones distintas que presentan los mismos componentes?
Como estarán pensando, no es posible distinguir a simple vista la diferencia entre estas soluciones. Los tres recipientes contienen soluciones del mismo soluto. Por lo tanto, la respuesta está en identificar a cada solución no por su composición, como hacemos en el caso de las sustancias, sino por su CONCENTRACIÓN: esto es, por la relación que existe (de masas o de volúmenes) entre los componentes o entre cada componente y la solución. En conclusión, la imagen de arriba muestra 3 soluciones que presentan los mismos componentes (dicromato de potasio y agua); sin embargo, estas soluciones NO son iguales entre sí, cada una presenta distinta concentración.
¿Cómo definimos la concentración de un componente en una solución?
Como la relación entre la cantidad (masa o volumen) de dicho componente, llamado soluto, y la cantidad (masa o volumen) del otro componente de la solución, llamado solvente, o la cantidad (masa o volumen) de la solución. Esto es:
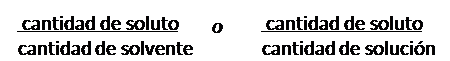
Existen diferentes formas de expresar la concentración y cada una de ellas tiene aplicaciones prácticas específicas, de modo que es habitual que se prefiera una forma de expresión a otra, según cada caso particular. Algunas formas comunes de expresar la concentración de las soluciones son las siguientes:
% m/m (porcentaje masa en masa): gramos de soluto (masa de soluto) que están presentes cada 100 g de solución.
% m/V (porcentaje masa en volumen): gramos de soluto (masa de soluto) que están presentes cada 100 mL de solución.
% V/V (porcentaje volumen en volumen): mL de soluto (volumen de soluto) que están presentes cada 100 mL de solución.
g/L: gramos de soluto (masa) presente por cada Litro (volumen) de solución.
molaridad (M): moles de soluto disueltos en 1 dm3 o 1 Litro (volumen) de solución.
molalidad (m): moles de soluto disueltos en
partes por millón (ppm): cantidad de unidades de una determinada sustancia (soluto) que hay por cada millón de unidades del conjunto.
Para reflexionar...
¿Cuál de estas maneras de expresar la concentración te resulta más familiar?
6. Ejemplos
Por ejemplo, la etiqueta de esta botella de alcohol indica que su concentración es 96 º, ¿qué significa que las botellas de alcohol medicinal tienen alcohol 96º?

El alcohol etílico o etanol es el compuesto que comúnmente llamamos alcohol. Las soluciones acuosas de etanol que poseen 96 °GL son las que se utilizan con fines medicinales (como el que tenés en el botiquín de tu casa). Una forma de expresar el porcentaje de alcohol presente en una bebida alcohólica son los grados Gay-Lussac (º GL). Esta medida es equivalente al % v/v (porcentaje volumen en volumen), es decir que una botella de alcohol medicinal con 98 º o 98 % v/v contiene 98 mL de alcohol por cada 100 mL de solución (mezcla homogénea de agua y alcohol).
Antes de continuar, te propongo que busques y reconozcas las distintas formas en que se expresa la concentración de ciertas sustancias en solución, por ejemplo, en etiquetas de bebidas o comidas que consumen, o en productos de limpieza o cosméticos.
7. Resolución de problemas: cuando el soluto está en estado líquido y el solvente es un líquido también
Veamos dos ejemplos de problemas donde el soluto es líquido y el solvente es líquido:
1. Calcular el volumen de vodka (40° GL) que es necesario consumir para que el alcohol en sangre sea suficiente para que un individuo se vea visiblemente ebrio (0,3 % v/v). Suponer 5 litros
ACLARACIÓN: para simplificar la resolución de este problema supondremos que todo el alcohol ingerido pasa directamente a la sangre, sin tener en cuenta que el organismo va metabolizando parte del mismo.
Analicemos juntos este problema:
Primero debemos calcular qué cantidad de alcohol representa 0,3 %. Si el volumen total de sangre considerado es 5 litros y teniendo en cuenta la definición de % v/v, planteamos una regla de tres simple de la siguiente manera:
100 ml sangre ---------------- 0,3 ml alcohol
5000 ml sangre ---------------- x = 15 ml alcohol
Ahora calculamos la cantidad de vodka que tiene ese volumen de alcohol disuelto. Partimos del dato de la graduación alcohólica “traducido”
40 ml alcohol ------------- 100 ml vodka
15 ml alcohol ------------- x = 37,5 ml vodka.
Rta: Es necesario consumir 37,5 ml de vodka.
ACLARACIÓN: notá la diferencia de volumen que se debe ingerir al cambiar la bebida. Aunque seguramente te resulta más sorprendente que el valor sea tan pequeño, aproximadamente un vaso (una medida) de vodka. Tené en cuenta que en realidad el alcohol no pasa directamente a la sangre cuando bebemos como nosotros consideramos al resolver los problemas. Una parte es metabolizada por el cuerpo y, por lo tanto, no afecta a nuestro sistema nervioso central. El alcohol que nos causa daño es el que circula por nuestra sangre y llega al cerebro modificando nuestra conducta y causando problemas a la salud con cada exceso. Cuanto mayor sea la diferencia entre el volumen de alcohol ingerido y el que el cuerpo puede metabolizar (aproximadamente
Veamos juntos otro ejercicio:
2. Una bebida que tiene una graduación alcohólica de 40 º GL, tiene 40 % v/v de alcohol (por ejemplo el whisky); un vino tinto, por lo general, tiene entre 11-16 % v/v de alcohol, y la graduación alcohólica de la cerveza puede variar entre 2,5-7,5 % v/v.
Analicemos juntos este problema:
Si un vino tiene 16 % v/v, quiere decir que cada 100 mL de vino (solución) hay 16 mL de alcohol etílico (soluto). Si una persona A toma 2 vasos de 200 mL, bebe un total de 400 mL de vino.
A. ¿Qué volumen de alcohol ha ingerido la persona A?
Primero debemos ¨traducir¨ los datos del problema:
La persona A ingirió un total de 400 ml de vino (porque bebió 2 vasos de 200 mL = 400 mL)
La graduación alcohólica del vino que tomo es 16 % v/v = significa que hay 16 ml de alcohol etílico (soluto) cada 100 ml de vino (solución). Entonces, podemos decir que la persona A ingirió 16 mL de alcohol cada 100 mL de vino que bebió y como bebió 400 mL de vino = 16 x 4= 64 ml de alcohol.
Si una cerveza tiene una graduación alcohólica de 7 % v/v, y otra persona B toma el mismo volumen (2 vasos de 200 mL) que la persona A,
B. ¿Qué volumen de alcohol etílico ha ingerido la persona B?
La persona B tomó el mismo volumen de cerveza (400 ml) y la graduación alcohólica es 7 % v/v;
esto significa que hay 7 ml de alcohol etílico cada 100 ml de cerveza. Entonces la persona B ingirió 7 x 4= 28 ml de alcohol.
Por lo tanto aunque ambas personas hayan tomado el mismo volumen total (400 mL) de cada bebida, no ingirieron el mismo volumen de alcohol... ¿Por qué? ¿Quién ingirió un mayor volumen de alcohol, la persona A o la B?
8. Más ejemplos... Cuando el soluto está en estado sólido y el solvente está en estado líquido
Vamos a ver cómo varia la concentración de un soluto sólido (por ejemplo una sal) en un solvente líquido (por ejemplo agua) con un simulador.
En la imagen de abajo pueden ver cómo pueden hacer para modificar los distintos parámetros del simulador: agregar agua, sal, variar la sal, etc.
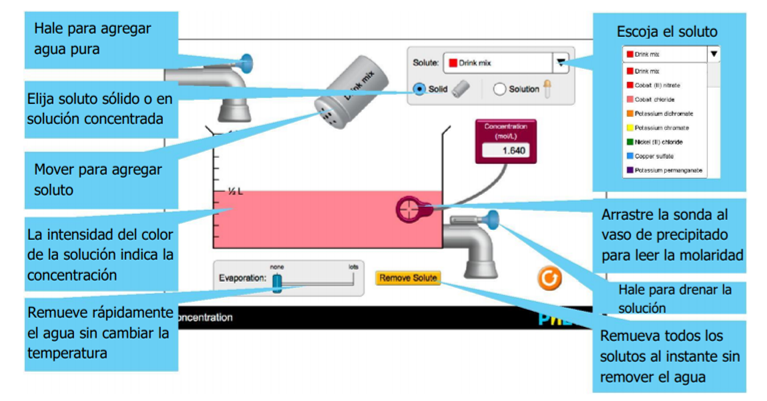
Pueden acceder al simulador desde aquí mismo para usarlo ustedes:
Cuando estén usando el simulador fíjense:
1. ¿Qué acciones incrementan la concentración de la solución?
2. ¿Qué acciones disminuyen la concentración de la solución?
3. ¿Qué acciones NO modifican la concentración de la solución?
4. Teniendo en cuenta esto, armen 2 soluciones de distinta concentración, una más concentrada y otra más diluida, utilizando la mezcla que quieran del simulador. Escriban la concentración de cada una de las soluciones que armaron indicando cuál es la más concentrada y cuál la más diluida, en las unidades que les da el simulador que son moles/Litro.
9. ¡Disolver y diluir NO son lo mismo!
Las palabras disolver y diluir son parecidas, pero hacen referencia a cosas distintas. Previamente vimos lo que es “disolver” un soluto sólido (por ejemplo sal) en un solvente líquido. ¿Pero qué pasa cuando tenemos una jarra de jugo por la mitad y no nos alcanza para convidar a todos los invitados? Y si, la solución más rápida, si no tenemos más jugo para preparar, es agregar un poco más de agua y….¡diluir el jugo! Como ven este concepto es muy cotidiano, y estoy segura que lo aún aplicado muchas veces en su vida cotidiana.
Entonces cuando a una solución de una determinada concentración le agregamos cierta cantidad de solvente, la diluimos. Hacemos que la concentración disminuya, es decir, vamos a obtener una solución de menor concentración, más diluida. ¿Por qué? Porque la relación soluto/solvente o soluto/solución se ve modificada. La cantidad de solvente aumenta y la cantidad de soluto se mantiene constante.
Veamos esto con el ejemplo que se muestra en la imagen de abajo. Supongamos que tenemos la solución A y queremos diluirla, entonces agregamos más solvente y obtenemos la solución B. Si la relación soluto/solvente en A era 5/7, al agregar más solvente obtenemos la solución B más diluida donde la relación soluto/solvente es 5/10. Es decir, el numerador se mantiene constante pero el denominador aumenta, por lo tanto el cociente es un número más chico:
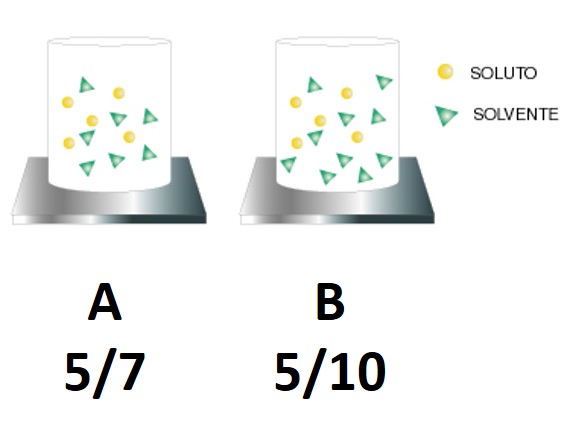
Debes tener en cuenta que la disminución de la concentración se debe (en este caso) al agregado de solvente, pero la cantidad de soluto permanece constante al agregar más solvente. Lo que sí cambia es la cantidad de solvente y por lo tanto también cambia el número TOTAL de partículas en solución, veamos:
En A = 5 de soluto + 7 de solvente = 12 de solución
En B= 5 de soluto + 10 de solvente = 15 de solución
Entonces, la solución B más diluida tendrá mayor volumen y masa total que la solución A más concentrada.
Volviendo al simulador que utilizaste previamente, ¿de qué otras formas se puede modificar la concentración de una solución para hacerla más concentrada o más diluida?
10. Ejemplos de diluciones
Es muy importante que puedan distinguir entre disolver un soluto y diluir una solución. Para que puedan comprender mejor este concepto veremos a continuación un ejemplo de dilución que utilizamos en la vida cotidiana.
Ejemplo: dilución de lavandina
En la etiqueta de lavandina “XXX” dice que la concentración de cloro activo en dicho producto es 55 g/l. El fabricante recomienda, en caso de usar lavandina como desinfectante general, diluir 58 ml de lavandina en
¿Lo resolvemos juntos?
Lo primero que debemos averiguar es la cantidad de cloro (soluto) que hay en 58 ml de lavandina (solución) porque será la misma cantidad que haya en la solución final: al agregar solvente, la masa de soluto permanece constante. La misma cantidad de cloro que hay disueltos en los 58 ml de lavandina es la que va a haber después de agregar un litro de agua, porque sólo agregamos solvente.
Entonces planteamos una regla de tres simple:
1 Litro = 1000 ml lavandina ------------
58 ml lavandina------------ x =
Dado que la indicación es diluir 58 ml de lavandina en
Entonces para averiguar la concentración de la solución diluida hallamos el cociente entre la cantidad de soluto (masa de soluto en gramos) y la cantidad de solución (el volumen en Litros), es decir, dividimos= 3,19 g de cloro/ 1,058 L = 3, 01 g/L. Como ven la concentración de cloro en la solución diluida es menor a la concentración en la solución inicial.
¿Calculamos la concentración de la solución diluida en %m/v?
1058 ml lav. -----------
100 ml lav. ------------- x =
Rta: 0,30 % m/v
Noten que 0,3 %m/v es equivalente a 3 g/L, solo son distintas formas de expresar la concentración de una solución.
11. Autoevaluación
Para seguir pensando y practicando los conceptos que vimos en este bloque, te proponemos realizar la siguiente actividad de auto-evaluación, a la que pueden acceder haciendo clic en Cuestionario.
|
Si no tenés un usuario creado en este campus no podés hacer las autoevaluaciones. Te dejamos las instrucciones para poder realizarlas:
|