Reacciones químicas y cálculos estequiométricos
2. ¿Cuál es la diferencia entre los cambios (o transformaciones) físicos y los químicos?
Durante los cambios físicos las sustancias permanecen inalteradas, es decir no cambian su identidad química, esto quiere decir que tenemos la misma sustancia antes y después de la transformación. Por ejemplo, se puede calentar hielo (agua sólida) y registrar la temperatura a la cual se transforma en agua líquida, pero el hielo difiere del agua líquida sólo en su estado físico, sigue siendo la misma sustancia (agua). Luego podríamos disminuir la temperatura y volver a formar hielo. Esto quiere decir que la sustancia que sufrió la transformación no ha cambiado, es la misma antes y después. Por lo tanto los cambios de estado (como ser el pasaje de sólido a líquido o de líquido a gaseoso, o viceversa) son ejemplos de cambios físicos, pero no son los únicos: la caída de un cuerpo, el paso de la corriente eléctrica por un alambre de cobre, la formación de soluciones (mezclas homogéneas), también.
¿Qué otros ejemplos de transformaciones físicas se les ocurren?
En cambio cuando ocurre un cambio químico, las sustancias que reaccionan se transforman, luego del cambio químico, en otras sustancias, distintas a las originales. Por ejemplo, en la combustión de un pedazo de madera, la madera se quema en presencia de oxígeno, y al final de la transformación química, solo queda el producto de la transformación: hollín o carbono sólido, y no es posible recuperar la madera original. Además durante la combustión se desprenden dióxido de carbono, vapor de agua y gran cantidad de energía en forma de luz (energía lumínica) y calor (energía calórica). Muchas veces durante los cambios químicos es común además percibir cambios de color, de olor, de sabor, aparición de un precipitado o de burbujas (efervescencias).
Podemos concluir que durante las reacciones químicas una o más sustancias se convierten en otra/s sustancias distinta/s. ¿Otros ejemplos de reacciones químicas que se les ocurran?
Veamos algunos ejemplos:

Cuando la manzana entra en contacto con el oxigeno (O2) del aire se oxida. Lo que vemos es un cambio de coloración, la manzana se pone marrón. Esta reacción ocurre con el hierro (presente en la manzana) y también con el hierro presente en distintas cosas, dando lugar a la herrumbre (como se muestra en la foto de abajo).

Las sustancias que intervienen en un cambio químico, decimos que participan de una reacción química. Estas reacciones se representan mediante una ecuación química. Éstas ecuaciones no son una descripción completa de lo que ocurre realmente durante la reacción, sino que por medio de ellas sólo se describe el cambio global, es decir, las sustancias que reaccionan (llamados reactivos) y los productos se obtienen después de la reacción (llamados productos). Retomando el ejemplo anterior, la oxidación del hierro se puede representar mediante la siguiente reacción química:
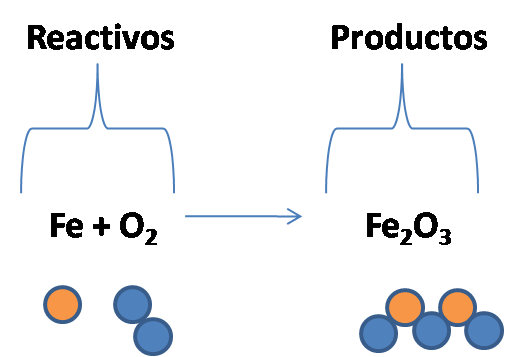
Por medio de esta ecuación química se representa el cambio químico que ocurre cuando el oxígeno gaseoso (O2) presente en el aire reacciona con el hierro (Fe) formando el óxido férrico (Fe2O3), también conocido como herrumbre. Esta reacción tiene un gran impacto económico, ya que aproximadamente un 5% de la producción de hierro se emplea en reponer el que se ha oxidado.