Soluciones
1. ¿Qué son las soluciones?
Las soluciones son mezclas homogéneas (es decir que presentan 1 única fase) cuyas propiedades intensivas se mantienen constantes en todo el sistema. Las mezclas son sistemas cuya composición es variable. No es posible escribir una fórmula química para representar una mezcla, porque una mezcla posee varios componentes (al menos dos). Las soluciones son mezclas compuestas por un soluto (o varios) y un solvente. Uno de los criterios que se utiliza para definir cuál de los componentes de la mezcla es el soluto y cuál es el solvente es designar al solvente como el componente que se encuentra en cantidad predominante, siendo el otro el soluto. El agua SIEMPRE se considera solvente, aún cuando está en menor proporción. Por ejemplo, en una solución acuosa que tiene 98% de etanol, el agua será el solvente y el alcohol el soluto.
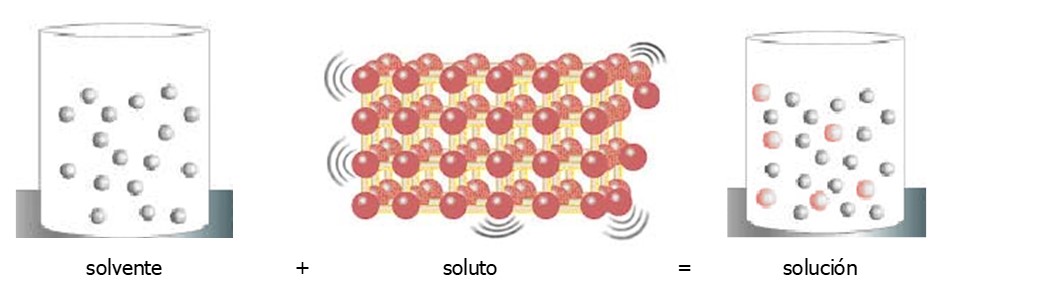
Veamos esto con un ejemplo de un solvente líquido y un soluto sólido:

Si nos imaginamos cómo se vería a nivel de las partículas, sería algo así:
En esta Tabla se indican distintos tipos de soluciones que pueden existir:
|
Soluto |
Solvente |
Estado de la solución resultante |
Ejemplos |
|
Gas |
Gas |
Gas |
Aire |
|
Gas |
Líquido |
Líquido |
Soda (CO2 disuelto en agua) |
|
Gas |
Sólido |
Sólido |
H2 gaseoso en paladio |
|
Líquido |
Líquido |
Líquido |
Alcohol en agua |
|
Sólido |
Líquido |
Líquido |
Sal en agua |
|
Sólido |
Sólido |
Sólido |
Aleaciones: bronce. |
Como pueden apreciar en la Tabla, el estado físico (sólido, líquido, gaseoso) de la MEZCLA del soluto y el solvente (lo que llamamos SOLUCIÓN o solución resultante en la Tabla) siempre coincide con el estado físico del SOLVENTE; es decir, si el solvente es líquido, la solución será líquida o si el solvente es gaseoso, la solución estará en estado gaseoso.
