Reacciones químicas y cálculos estequiométricos
| Sitio: | Campus Claves Académica |
| Curso: | Química - EnlaceUBA |
| Libro: | Reacciones químicas y cálculos estequiométricos |
| Imprimido por: | Invitado |
| Día: | domingo, 17 de mayo de 2026, 03:14 |
Tabla de contenidos
- 1. Introducción
- 2. ¿Cuál es la diferencia entre los cambios (o transformaciones) físicos y los químicos?
- 3. ¿Cómo se escribe una ecuación química?
- 4. ¿Qué significa que las ecuaciones químicas deben estar balanceadas?
- 5. ¿Cómo se leen las ecuaciones químicas?
- 6. Para poner en práctica lo aprendido - PARTE 1
- 7. Reacciones de Combustión
- 8. Reacciones de combustión completas e incompletas
- 9. Reactivo limitante y reactivo en exceso
- 10. Para poner en práctica lo aprendido - PARTE 2
- 11. Autoevaluación
- 12. Tu opinión nos sirve
1. Introducción
Una de las características más notables del mundo que nos rodea es que continuamente se están produciendo cambios de todo tipo: el hierro se oxida, la sal se disuelve, el agua se evapora, cocinamos los alimentos, se queman, a veces catastróficamente, los bosques... Y también la industria química produce nuevos materiales para aumentar nuestro confort o mejorar nuestra salud. Por otra parte, en nuestro organismo se producen en todo momento cambios.
Durante el recorrido de este bloque vamos a estudiar qué ocurre durante estos cambios, comenzando por diferenciar los cambios que llamamos cambios físicos de los cambios químicos.
2. ¿Cuál es la diferencia entre los cambios (o transformaciones) físicos y los químicos?
Durante los cambios físicos las sustancias permanecen inalteradas, es decir no cambian su identidad química, esto quiere decir que tenemos la misma sustancia antes y después de la transformación. Por ejemplo, se puede calentar hielo (agua sólida) y registrar la temperatura a la cual se transforma en agua líquida, pero el hielo difiere del agua líquida sólo en su estado físico, sigue siendo la misma sustancia (agua). Luego podríamos disminuir la temperatura y volver a formar hielo. Esto quiere decir que la sustancia que sufrió la transformación no ha cambiado, es la misma antes y después. Por lo tanto los cambios de estado (como ser el pasaje de sólido a líquido o de líquido a gaseoso, o viceversa) son ejemplos de cambios físicos, pero no son los únicos: la caída de un cuerpo, el paso de la corriente eléctrica por un alambre de cobre, la formación de soluciones (mezclas homogéneas), también.
¿Qué otros ejemplos de transformaciones físicas se les ocurren?
En cambio cuando ocurre un cambio químico, las sustancias que reaccionan se transforman, luego del cambio químico, en otras sustancias, distintas a las originales. Por ejemplo, en la combustión de un pedazo de madera, la madera se quema en presencia de oxígeno, y al final de la transformación química, solo queda el producto de la transformación: hollín o carbono sólido, y no es posible recuperar la madera original. Además durante la combustión se desprenden dióxido de carbono, vapor de agua y gran cantidad de energía en forma de luz (energía lumínica) y calor (energía calórica). Muchas veces durante los cambios químicos es común además percibir cambios de color, de olor, de sabor, aparición de un precipitado o de burbujas (efervescencias).
Podemos concluir que durante las reacciones químicas una o más sustancias se convierten en otra/s sustancias distinta/s. ¿Otros ejemplos de reacciones químicas que se les ocurran?
Veamos algunos ejemplos:

Cuando la manzana entra en contacto con el oxigeno (O2) del aire se oxida. Lo que vemos es un cambio de coloración, la manzana se pone marrón. Esta reacción ocurre con el hierro (presente en la manzana) y también con el hierro presente en distintas cosas, dando lugar a la herrumbre (como se muestra en la foto de abajo).

Las sustancias que intervienen en un cambio químico, decimos que participan de una reacción química. Estas reacciones se representan mediante una ecuación química. Éstas ecuaciones no son una descripción completa de lo que ocurre realmente durante la reacción, sino que por medio de ellas sólo se describe el cambio global, es decir, las sustancias que reaccionan (llamados reactivos) y los productos se obtienen después de la reacción (llamados productos). Retomando el ejemplo anterior, la oxidación del hierro se puede representar mediante la siguiente reacción química:
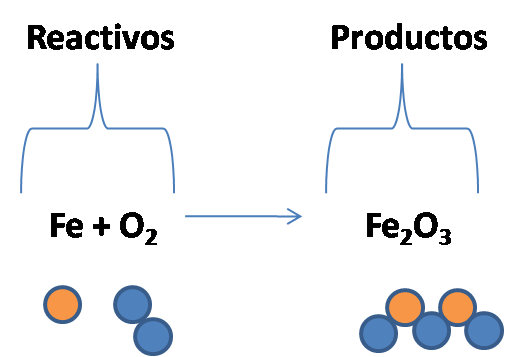
Por medio de esta ecuación química se representa el cambio químico que ocurre cuando el oxígeno gaseoso (O2) presente en el aire reacciona con el hierro (Fe) formando el óxido férrico (Fe2O3), también conocido como herrumbre. Esta reacción tiene un gran impacto económico, ya que aproximadamente un 5% de la producción de hierro se emplea en reponer el que se ha oxidado.
3. ¿Cómo se escribe una ecuación química?
Por convención, los reactivos (que pueden ser una o más sustancias) se escriben a la izquierda de la flecha y los productos (que también pueden ser una o más sustancias) a la derecha de la flecha, de la siguiente manera:
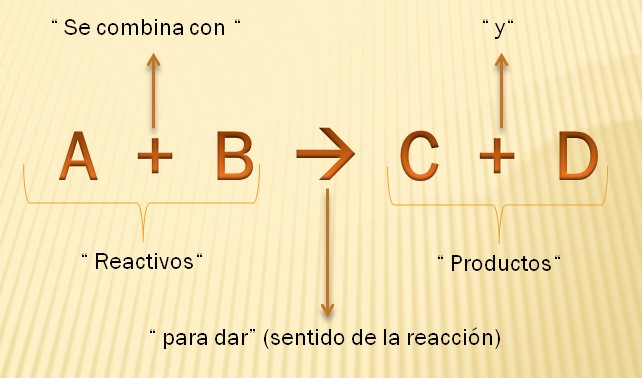
Las ecuaciones químicas nos dan información cualitativa acerca de cuáles son las sustancias que reaccionan entre sí y cuáles son los productos se obtienen. Cuando más de un reactivo reacciona entre sí y/o se obtiene más de un producto, se indica con un signo más (+) entre ellos.
Las ecuaciones químicas también nos dan información cuantitativa porque nos indican la proporción en que los reactivos reaccionan entre sí para originar los productos.
4. ¿Qué significa que las ecuaciones químicas deben estar balanceadas?
Siguiendo el Principio de conservación de las masas (propuesta por el químico Antoine Lavoisier) en todo sistema cerrado la masa se mantiene constante cualesquiera sean las transformaciones físicas o químicas que en él se produzcan. Este principio se basa en que la materia no puede ser ni creada ni destruida, entonces la sumatoria de las masas de los reactivos debe coincidir con la sumatoria de las masas de los productos. Por lo tanto, para que una reacción química refleje este principio debe estar correctamente balanceada; esto es, el número de átomos de cada clase debe ser igual del lado de los reactivos y de los productos. Dicho de otra forma, si en una reacción química ocurre un re ordenamiento de los átomos para que se formen nuevas sustancias, y los átomos tienen una cierta masa, entonces para que una reacción química cumpla el principio de conservación de las masas, el número y tipo de átomos que reaccionan inicialmente (masa inicial) deben estar al final de la reacción (masa final). ¿Están de acuerdo?
Analicemos como ejemplo la misma ecuación de oxidación del hierro que vimos antes:
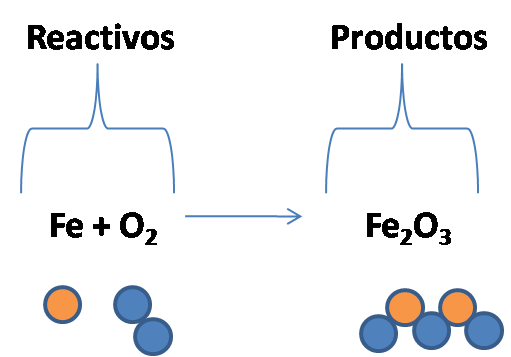
En este caso estamos representando el átomo de Fe (hierro) con una círculo naranja y el átomo de O (Oxígeno) con una círculo azul. Noten que dos átomos de Oxígeno (O) forman 1 molécula de Oxígeno (O2).
Para que la ecuación esté correctamente escrita, tiene que estar BALANCEADA, esto es, el número y tipo de átomos que están al inicio de la reacción, deben estar al final de la misma, ya que nada se crea ni se destruye, sino que se transforma.
¿Pero cómo logramos BALANCEAR la ecuación? Colocando coeficientes (números) DELANTE de la fórmula de las sustancias para lograr la igualdad de átomos de cada tipo a ambos lados de la reacción; es decir, del lado de los reactivos y del lado de los productos el número de átomos de cada tipo debe ser el mismo.
Por ejemplo:
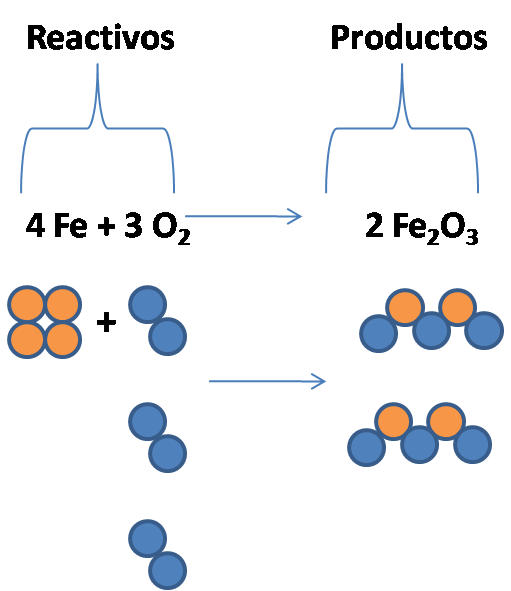
Colocando estos números delante de las fórmulas de las sustancias, logramos que tanto del lado de los reactivos como del lado de los productos haya 4 átomos de Fe (Hierro) y 6 átomos de O (Oxígeno). De esta manera la ecuación queda correctamente balanceada (cuenten el número de pelotitas naranjas y azules a ambos lados de la ecuación según indican los números DELANTE de las fórmulas moleculares).
¡OJO! Esos coeficientes o números que colocamos para igualar o balancear la ecuación solo pueden ubicarse delante de la fórmula química de cada una de las sustancias. Por ejemplo, el 3 delante de la molécula de O2, indica que se ponen a reaccionar 3 moléculas de Oxígeno: 3 O2. Esos números o coeficientes estequiométricos que colocamos para balancear la ecuación NO pueden colocarse en forma de subíndices, porque en ese caso estaríamos modificando el número de átomos de la molécula y estaríamos cambiando la identidad química de la molécula. Por ejemplo: O3, en ese caso ya no se trataría de la molécula de Oxígeno O2, sino de otra molécula llamada Ozono (O3).
Es importante destacar que los números que se colocan delante de las moléculas para balancear la ecuación es lo que tenemos que ir cambiando, hasta lograr igualar el número de átomos de cada tipo del lado de los productos y del lado de los reactivos. Este método que utilizamos para balancear esta ecuación se denomina ¨método de tanteo¨ y funciona bien para ecuaciones sencillas; sin embargo, para ecuaciones más complejas, que escapan a los objetivos de este curso, conviene muchas veces balancear las ecuaciones químicas por otro método, llamado ¨método algebraico¨.
5. ¿Cómo se leen las ecuaciones químicas?
Analicemos un poco más en detalle la ecuación anterior...
4 Fe + 3 O2 ----------------> 2 Fe2O3
En esta reacción en términos CUANTITATIVOS lo que ocurre es que:
4 átomos de Hierro (Fe) reaccionan con 3 moléculas de Oxígeno (O2) para formar 2 unidades fórmula de Óxido de Hierro (Fe2O3).
Pero, ¿normalmente hablamos de las sustancias que reaccionan en términos de moléculas y átomos? ¿Se puede pesar en una balanza convencional la masa de 1 átomo?
Las respuestas a las preguntas planteadas arriba es NO. No se puede pesar en una balanza convencional la masa de 1 átomo o 1 molécula. La masa de los átomos y las moléculas son muy pequeñas comparadas con las masas que manejamos habitualmente.
Esto hace imposible medirlas con las balanzas convencionales y en las unidades habituales como kg, g e incluso mg que resultan demasiado grandes para que sean de utilidad.
Tanto en nuestra vida diaria como en el laboratorio usamos muestras de sustancias que contienen una enorme cantidad de átomos, moléculas o iones. Como ya dijimos, estas partículas tienen masas muy pequeñas y no existen balanzas que puedan pesarlas en forma individual. Por lo tanto, es conveniente utilizar una unidad especial que sirva para describir una cantidad de átomos o moléculas muy grande. Esta unidad es el MOL.
Un mol es una unidad que emplean los químicos para describir una cantidad muy grande de átomos o moléculas. Así como una docena se refiere a 12 unidades (de huevos, facturas, etc.) o 1 centena se refiere a 100 unidades (de alfajores, bolillas, etc.),
1 mol corresponde a 6,02. 1023 partículas (átomos o moléculas o iones),
siendo 6,02. 1023 igual a
602.000.000.000.000.000.000.000
Por definición, 1 mol equivale al número de átomos que hay en 12 g de Carbono de A= 12.
Entonces, en 1 mol hay siempre 6,02. 1023 (este número se llama número de Avogadro o constante de Avogadro) partículas; en nuestro caso serán moléculas o átomos o iones. Notar que NO estamos hablando de 1 molécula o 1 átomo, sino de moles, es decir un número muy grande, que describe ¡millones de átomos o moléculas!
¿Cómo se calcula la masa de un mol de sustancia?
La masa de 1 mol de átomos o 1 mol de moléculas coincide numéricamente con su Ar (masa atómica relativa, que figura en la Tabla Periódica de los Elementos para cada tipo de elemento) o con su Mr (masa molecular relativa) que resulta de la suma de las masas atómicas de los átomos que forman la molécula, pero lleva unidad de gramos.
Esto es un lio de palabras nuevas, lo sé, pero miren los ejemplos que siguen y van a ver que es más fácil de lo que parece.
¿Cómo calculo la masa de un mol de átomos?
Fíjense, dijimos que la masa de un mol de átomos es numéricamente igual a la masa atómica relativa (Ar) pero lleva unidad de gramos.
Por ejemplo:
Ar Na = 23 y la masa molar (la masa de un mol de átomos) de Na es igual a 23 g.
¿Y cómo calculo la masa de un mol de moléculas?
La masa de un mol de moléculas es numéricamente igual a su masa molecular relativa (Mr), que puede determinarse sumando las masas atómicas de los elementos que la componen, pero lleva unidad de gramos.
Por ejemplo:
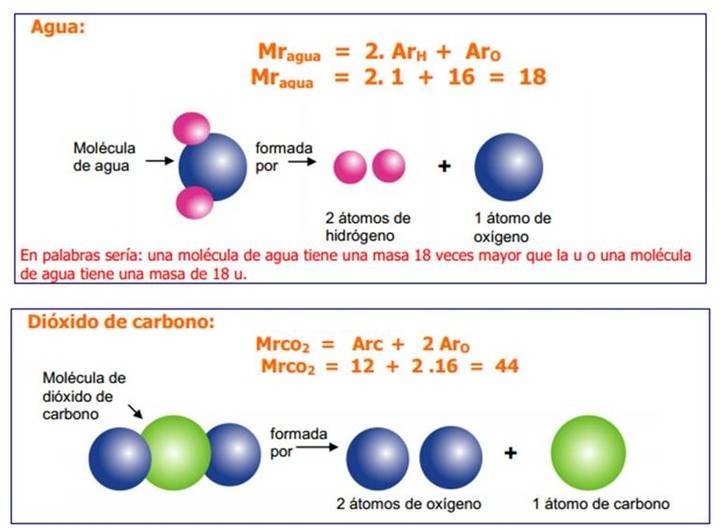
Mr del agua = 18, y la masa molar del agua es igual a 18 g.
Mr del dióxido de carbono = 44, y la masa molar del dióxido de carbono es igual a 44 g.
6. Para poner en práctica lo aprendido - PARTE 1
Para trabajar con el simulador, en primer lugar debes clickear en INTRODUCCIÓN.
Antes de comenzar, seguí las siguientes instrucciones:
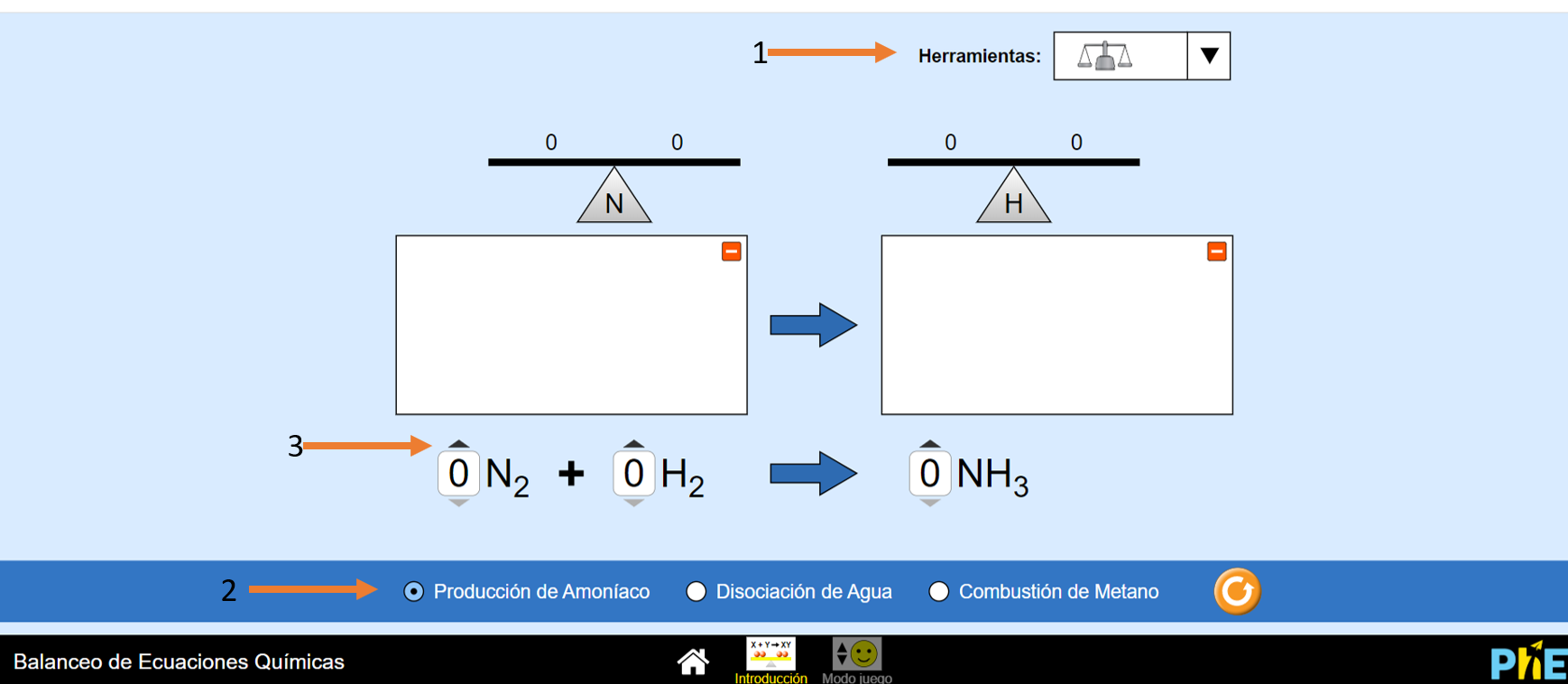
1) En herramientas selecciona la imagen de la BALANZA (como se muestra en la captura de pantalla, en la imagen de abajo, con la flecha naranja 1).
2) En la PARTE INFERIOR de dicha página web podes seleccionar la reacción a practicar: producción de amoníaco, disociación del agua o combustión del metano. ELEGÍ UNA A LA VEZ.
3) Inicialmente los coeficientes estequiométricos se encuentran con un valor cero. Con las flechas hacia arriba o hacia abajo podes aumentar el número de cada tipo de molécula en la reacción.
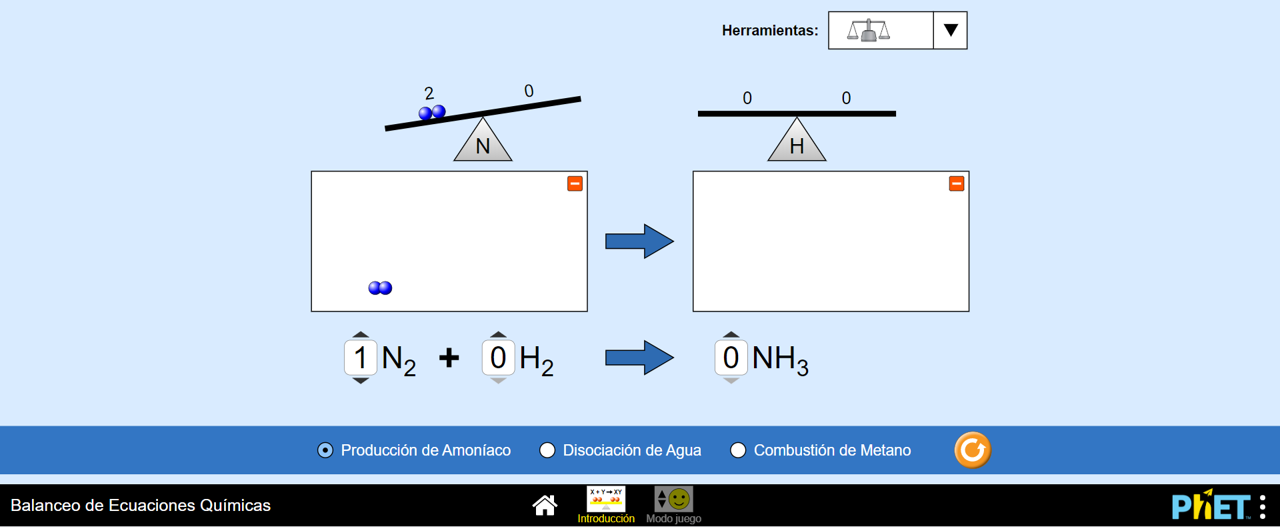
Por ejemplo, poniendo un 1 a la izquierda de cada fórmula química, estamos agregando una molécula de nitrógeno (N2) en la reacción, por lo tanto aparecen los dos átomos de Nitrógeno (N) que forman la molécula (representados con bolitas azules):
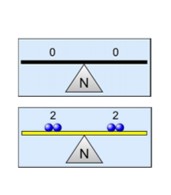
Recuerden que el objetivo al balancear ecuaciones químicas es obtener el MISMO NÚMERO Y TIPO DE ÁTOMOS A AMBOS LADOS DE LA ECUACIÓN, de manera que se cumpla el principio de CONSERVACIÓN DE LA MATERIA. Es decir para lograr balancear las ecuaciones del simulador deben modificar los coeficientes estequiométricos hasta que todas las balanzas queden en equilibrio. Al lograrlo, la flecha azul se colorea de amarillo y aparece una “carita feliz”. Por ejemplo, en el caso de la reacción que se muestra arriba, deben cambiar los coeficientes estequiométricos de manera tal de lograr igualar el NUMERO DE ATOMOS DE N (Nitrógeno) y EL NUMERO DE ATOMOS DE H (Hidrógeno) del lado de los reactivos y del lado de los productos (por eso tienen una balanza para N y una balanza para H en la parte superior de la pantalla). ACLARACIÓN: las balanzas aparecen en equilibrio cuando todos los coeficientes son cero (al inicio), aunque la ecuación no esté balanceada. Cuando la ecuación está balanceada, las balanzas también están en equilibrio, pero se vuelven amarillas para resaltar la diferencia:
Ahora sí ya están listxs para comenzar a practicar el balanceo de estas ecuaciones químicas. Recuerden cuando hayan balanceado correctamente una ecuación aparecerá una cara feliz en la pantalla :)
Utilizando este simulador pueden balancear las siguientes tres reacciones: 1. producción de amoníaco, 2. disociación de agua y 3. combustión de metano. Luego, pueden seguir practicando usando el simulador en MODO JUEGO, desde la página de inicio. Fíjense que en el modo JUEGO pueden seleccionar distintos niveles de dificultad.
7. Reacciones de Combustión
Como vimos previamente, durante las reacciones químicas se rompen enlaces químicos (que mantienen unidos a los átomos o iones en las moléculas o compuestos iónicos) en las sustancias que reaccionan (llamados reactivos), éstos se reordenan y forman nuevos enlaces que darán origen a sustancias distintas (que serán los productos). Las reacciones químicas se representan por medio de ecuaciones químicas; en estas solo se indica globalmente lo que está ocurriendo en la reacción.
También dijimos que para que las ecuaciones químicas estén correctamente escritas deben estar siempre correctamente balanceadas. Tanto en la combustión como en la respiración se produce una reacción química donde uno de los reactivos es el oxígeno (O2), por eso este tipo de reacciones se denominan oxidaciones.
Ahora bien, ¿qué reactivos son necesarios para que se produzca una combustión?
En primer lugar se necesita un combustible, la sustancia que arde o se quema, por ejemplo la madera. En la imagen de abajo pueden ver distintos tipos de combustibles:

¿Qué otros combustibles utilizas con frecuencia? Escribí en tu cuaderno 3 ejemplos.
Pero con el combustible solo no alcanza, ¿qué más se necesita para que el combustible resulte útil y se produzca una reacción de combustión?
Para ayudarte a responder te proponemos que realices el siguiente experimento:
1. Encende una vela y obsérvela al comenzar y luego de varios minutos.
¿Qué se quema de la vela, la cera o el pabilo?
2. Tapa la vela con un vaso de vidrio y encendé una segunda vela, de la siguiente manera:
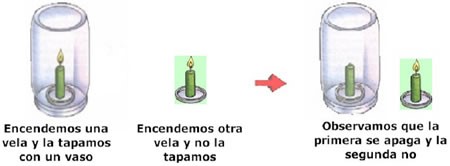
Responde:
¿Qué ocurre con la vela que está tapada con el vaso luego de unos minutos?
Observe las paredes del vaso. ¿Cómo están? ¿Por qué se apaga la vela si se le quita el aire?
Las actividades realizadas, junto con tu experiencia con diferentes formas de combustión, te habrán llevado a algunas conclusiones importantes respecto del proceso que estamos analizando. Para que se produzca la combustión, se necesita no sólo un combustible sino además aire que provee el comburente, la sustancia que permite que se produzca la combustión, y una temperatura de ignición (en el caso de la vela, dada por el fósforo encendido) para que el sistema combustible-comburente llegue a la temperatura necesaria para continuar por sí solo la reacción. Se dice que un material combustible es más inflamable que otro si comienza a arder a una temperatura más baja.
Podemos entonces concluir que la combustión requiere la presencia de aire, tal como lo necesita un ser vivo para respirar. Estos resultados nos hacen pensar que puede haber cierta semejanza entre la respiración y la combustión...
No cabe duda, el aire juega un importante papel en estos procesos; pero, en realidad, ¿es todo el aire o sólo una parte de él, la que interviene en los procesos de respiración y de combustión? Al apagarse la vela, ¿no quedó nada de aire en el frasco?, ¿todo el aire que contenía el frasco se gastó en la combustión de la vela?
Es posible responder a estas preguntas, y comprobar mediante experimentos que se ha consumido tan solo una parte del aire que estaba encerrado en el frasco: se trata del oxígeno (cuya fórmula molecular es O2), uno de los componentes de la mezcla gaseosa que denominamos aire.
Como productos de las reacciones de combustión en general, se obtienen agua, dióxido de carbono (CO2) y energía lumínica (luz) y térmica (calor). En forma general podemos escribir una ecuación para las reacciones de combustión de la siguiente manera:
COMBUSTIBLE + COMBURENTE -------> PRODUCTOS + ENERGÍA
En conclusión:
- Combustible es toda sustancia capaz de arder en presencia de oxígeno;
- La respiración y la combustión son procesos en los que se produce una reacción química con el oxígeno, en términos químicos se las llama reacciones de OXIDACIÓN;
-
En la combustión se libera una importante cantidad de energía, que se transfiere a otros sistemas en forma de calor. Por eso se dice que se trata de un proceso exotérmico (exo: hacia fuera; térmico: calor). De manera general cuando se libera energía en cualquier forma que sea, el proceso se denomina exergónico.
8. Reacciones de combustión completas e incompletas
Si suponemos que, por ejemplo, se quema carbón (el combustible) en presencia de oxígeno (el comburente) estas sustancias son los reactivos o sustancias iniciales. Como resultado de este proceso se obtiene una sustancia nueva, dióxido de carbono, el producto o sustancia final. La ecuación química más sencilla que corresponde a este proceso es la siguiente:
C + O2 -----------------> CO2
En general, los combustibles que se utilizan a diario son sustancias que no están formadas sólo por carbono. El gas natural, por ejemplo es una mezcla de dos hidrocarburos: el metano (CH4) y el etano (C2H6). Cuando se produce la COMBUSTIÓN COMPLETA de estos hidrocarburos, se forman dos sustancias: dióxido de carbono (CO2) y agua (H2O). También se libera energía en forma de calor, es decir se trata de otro ejemplo de reacción exotérmica. La llama de color azul-celeste indica que la combustión es completa. Esta reacción se puede representar utilizando modelos moleculares o mediante una ecuación química (abajo):
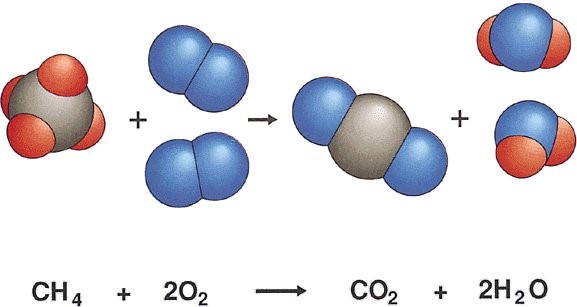
Los enlaces entre los átomos de C (representados con bolitas grises) e H (representados con bolitas rojas) del metano (CH4) y los átomos de O (representados con bolitas azules) en las moléculas de oxígeno (O2) se separan para luego formar nuevos enlaces. Es decir, durante la reacción química los átomos se reordenan (se rompen enlaces y crean nuevos enlaces) formando sustancias diferentes a las que reaccionan. En este caso la energía necesaria para romper los enlaces en las moléculas reaccionantes es menor a la que se libera al formar los enlaces en las sustancias producto de la reacción y por eso la reacción es exotérmica (es decir que se libera energía en esta reacción en forma de CALOR). Noten además que esta ecuación esta escrita en forma BALANCEADA.
Si, en cambio, la cantidad de comburente (oxígeno) disponible NO es suficiente, se produce lo que se denomina una COMBUSTIÓN INCOMPLETA, que da lugar a la producción de otro compuesto, el peligroso monóxido de carbono, cuya fórmula molecular es CO. La llama de color amarillo-naranja indica una combustión incompleta.
La ecuación será entonces: C + O2 -----------------> 2 CO
En conclusión, una combustión completa de hidrocarburos da como productos dióxido de carbono y agua, pero como vimos, pueden producirse también combustiones incompletas si la cantidad de oxígeno no es suficiente. En estos casos aparecen otros productos: el peligroso monóxido de carbono, CO, y eventualmente partículas de carbono que se desprenden y son las responsables del tiznado que aparece en las ollas. Si observas tu cocina, podrás notar que cuando la llama que produce es amarilla, se ensucian tus ollas; en cambio, si la llama que se obtiene es azul clara, esto no sucede. Efectivamente, el color amarillo se debe a la presencia de partículas de carbón que no han formado óxidos, se desprenden y se ponen incandescentes. Cuando notes que la llama de tu cocina, estufa o calefón comienza a tomar un color amarillo muy luminoso, debes destapar los quemadores (destapar los agujeritos que permiten la entrada de aire) ya que ese hecho está indicando que la combustión no es completa y que, consecuentemente es muy probable que se esté formando monóxido de carbono. Por otra parte, la combustión incompleta libera menor cantidad de calor que la completa (pero mayor cantidad de luz), por lo que para obtener una determinada cantidad de calor, se gasta más combustible que si la combustión fuese total.
¿Por qué es peligroso el monóxido de carbono?
Porque es inodoro (no tiene olor) e incoloro (no se ve) y es sumamente tóxico. Por eso todos los inviernos nos recomiendan revisar el color de la llama de estufas, quemadores, calefones, cocinas, etc. Los síntomas de la intoxicación con CO (monóxido de carbono) dependen de la cantidad de CO que existe en el ambiente. Como se trata de un gas fácilmente difusible, los niveles de CO en un ambiente cerrado aumentan rápidamente si la fuente de emisión de CO se mantiene activa. Cuando la concentración es baja, puede demorarse entre cinco y seis horas en aparecer los síntomas. Normalmente, los tejidos que necesitan mucha energía para funcionar (como el cerebro y el corazón) serían los primeros en afectarse y en mayor grado que otros.
A su vez, la falta de oxígeno puede ser tan grave como la presencia de monóxido de carbono, ¡por eso es importante mantener siempre ventiladas las habitaciones!
¡¡PARA RECORDAR!! Las reacciones de combustión pueden ser completas o incompletas; si la cantidad de oxígeno es insuficiente decimos que la combustión es incompleta, y si la cantidad de oxígeno es suficiente las reacciones de combustión son completas. En el último caso, se produce dióxido de carbono como producto y la llama que se observa es color celeste- azul; en el caso de las combustiones incompletas se produce monóxido de carbono como producto y la llama que se observa es color amarillo.
9. Reactivo limitante y reactivo en exceso
Retomemos la ecuación correspondiente a la combustión del metano. Ya sabemos que los productos de la combustión completa de este gas son dióxido de carbono y agua, de manera que la ecuación balanceada es:
CH4 + 2 O2 -----------------> CO2 + 2 H2O
Podemos leer esta ecuación de la siguiente manera: “una molécula de metano reacciona con dos moléculas de oxígeno para producir una molécula de dióxido de carbono y dos moléculas de agua”.
Pero en la realidad nunca se trabaja con una molécula sino con grandes cantidades de ellas. La ecuación nos indica la proporción entre las diferentes sustancias que intervienen en la reacción, sea una molécula o millones de ellas. Y es aquí donde interviene el CONCEPTO DE MOL: podemos interpretar la ecuación en función de moles de moléculas, leyendo “un mol de moléculas de metano reacciona con dos moles de moléculas de oxígeno produciendo un mol de moléculas de dióxido de carbono y dos moles de moléculas de agua”. Ahora nos estamos refiriendo a enormes cantidades de moléculas, con una gran ventaja: podemos traducir estas cantidades de moléculas a masas de sustancia, puesto que sabemos (o podemos calcular) la masa molar de cada sustancia, a partir de los datos de masas atómicas que aparecen en
En conclusión:
- Desde el punto de vista molecular podemos leer esta ecuación de la siguiente manera: 1 molécula de metano reacciona con 2 moléculas de oxígeno para producir 1 molécula de dióxido de carbono y 2 moléculas de agua.
- Desde el punto de vista molar, la reacción se puede leer: 1 mol de moléculas de metano reacciona con 2 moles de moléculas de oxígeno para producir 1 mol de moléculas de dióxido de carbono y 2 moles de moléculas de agua. ESTA FORMA ES LA MÁS UTILIZADA.
Como podemos ver las ecuaciones químicas no solo nos indican quienes son los reactivos y quienes son los productos, sino que además nos dan información CUANTITATIVA, ya que por medio de las ecuaciones BALANCEADAS podemos saber en QUE PROPORCIÓN REACCIONAN LOS REACTIVOS Y CUANTO OBTENEMOS DE CADA PRODUCTO.
Ahora bien, en los laboratorios o en las industrias no siempre se realizan las reacciones usando las cantidades exactas de reactivos que indican la ecuación balanceada. Generalmente, se usa uno de ellos (el más barato, por ejemplo) en exceso. En este caso, el otro reactivo, el que se encuentre en menor proporción, limitará la cantidad de producto que vamos a obtener, de allí que se llame REACTIVO LIMITANTE.
Veamos el concepto de reactivo limitante con una analogía gastronómica:
Supongamos que está armando alfajores. Los reactivos son las tapas de masa, el dulce de leche, el coco. El producto obtenido, son los alfajores terminados. Para cada alfajor, se necesitan dos tapas de masa, cierta cantidad de dulce de leche (para los golosos una cantidad grande!!!) y cierta cantidad de coco. Suponemos que tenemos dulce de leche y coco en exceso (porque nos han regalado varios tarros de dulce y varios paquetes de coco),…esto quiere decir que terminaras de armar los alfajores (y de esto dependerá el número de alfajores que puedas armar) cuando se terminen las tapas de masa. En este caso, diremos que las tapas son el reactivo limitante.
Recordemos algo más sobre la información que se puede obtener a partir de las ecuaciones químicas:
- al final de la reacción tendremos la misma masa de sistema, aunque las sustancias que lo forman sean diferentes de las iniciales (Ley de Conservación de la masa).
- a partir del modelo atómico-molecular y el concepto de mol, es posible interpretar un cambio químico a diferentes niveles: la ecuación correspondiente nos permite visualizar cómo se reordenan los átomos de los reactivos para dar lugar a los productos y también nos permite realizar cálculos con masas de sustancia, que podemos medir en una balanza.
10. Para poner en práctica lo aprendido - PARTE 2
Ahora vamos a trabajar con otro simulador para que puedan:
- Reconocer que los átomos se conservan durante una reacción química;
- Ver en una experiencia cotidiana concreta (como lo es el armado de sándwiches) qué significa el concepto de reactivo limitante en una reacción química;
- Identificar el reactivo limitante en una reacción química, según la cantidad de reactivos y el número de moléculas que se indica en la ecuación química balanceada.
En primer lugar, les proponemos que utilicen el simulador para armar sandwiches y para entender cómo pueden hacer muchos sandwiches diferentes con distintas cantidades de ingredientes. Para ello, realicen la siguiente actividad:
Desde la pantalla del simulador, clickeen donde dice SANDWICHES y elijan en la parte superior derecha la opción ¨queso¨. Les aparecerá la siguiente ¨ecuación¨:
2 REBANADAS DE PAN + 1 QUESO --> 1 “PAN CON QUESO"
A partir de dicha ecuación, analicen y respondan las situaciones siguientes:
Si antes de la reacción se cuenta con 2 quesos (usen las flechas para aumentar el número de fetas de queso antes de la reacción) y:
I) 2 rebanadas de pan (usen las flechas para aumentar el número de panes antes de la reacción), ¿cuántos sandwiches se podrán preparar?, ¿sobrará alguna pieza después de la reacción? ¿cuántas?
II) 5 rebanadas de pan (usen las flechas para aumentar el número de panes antes de la reacción), ¿cuántos sandwiches se podrán preparar ahora?, ¿sobrará alguna pieza después de la reacción? ¿cuántas?
III) En cada caso (I y II) establezcan el REACTIVO LIMITANTE.
A partir de esta primera práctica podemos concluir que:
- El reactivo limitante es siempre aquél que se agota primero en la reacción;
- El reactivo en exceso es aquel que no se agota por completo durante la reacción;
- La cantidad de producto que se obtenga de la reacción dependerá siempre de la cantidad de reactivo limitante disponible.
Continúen la práctica realizando las siguientes ACTIVIDADES:
ACLARACIÓN IMPORTANTE: para la resolución de estas actividades es importante que, en primer lugar, piensen y anoten la respuesta, es decir hagan una predicción, y luego, en segundo lugar, comprueben mediante el uso del simulador, si su predicción fue acertada o no.
1) Seleccionen cliqueando donde dice SÁNDWICHES en la pantalla principal del simulador (arriba)
2) Seleccionen “queso” en la parte superior derecha
¿Cuántos sándwiches pueden hacer si tenemos 6 rodajas de pan y 4 fetas de queso? ¿qué sobra?
3) Piensen la respuesta y anotenla. Luego comprueben si su predicción fue correcta usando el simulador:
PREDICCIÓN: comprobación:
4) Seleccionen “personalizado” en la parte superior derecha y los ingredientes de manera tal que los sándwiches estén hechos con 2 fetas de queso y 2 rodajas de pan:
¿Cuántos sándwiches pueden hacer si tienen 6 rodajas de pan y 4 fetas de queso?, ¿qué sobra?
PREDICCIÓN: comprobación:
5) Contesta:
¿Por qué el número de sándwiches que hemos podido hacer ha cambiado, aunque teníamos la misma cantidad de pan y queso?
Ahora seleccionen MOLÉCULAS en la pantalla principal del simulador.
ACLARACIÓN IMPORTANTE: noten que en el simulador SIEMPRE trabajamos las cantidades de sustancias en términos de moléculas y no con MOLES DE MOLÉCULAS, simplemente porque sería imposible para el simulador representar millones de moléculas (moles de moléculas) con pelotitas. Sin embargo, como les mencione antes, en la práctica cotidiana siempre hablamos y leemos las cantidades de sustancias presentes en las reacciones químicas en MOLES (porque en la práctica es imposible contar moléculas como lo hacemos en forma esquemática en el simulador).
6) Seleccionen la opción “hacer agua” en la parte superior derecha.
En la formación de agua intervienen moléculas de hidrógeno (H2) y de oxígeno (O2) en unas determinadas proporciones. Es una reacción de SÍNTESIS.
7) Antes de simular nada intenta hacer tus propias predicciones, y una vez que hayas hecho tu predicción, usa las flechas para aumentar/disminuir el número de moléculas de los reactivos y comprobar la veracidad de tu predicción con el simulador.
8) ¿Cuántas moléculas de agua podemos hacer si tenemos 6 moléculas de H2 (hidrógeno) y 4 moléculas de O2 (oxígeno)? ¿qué sobra?
PREDICCIÓN: comprobación:
9) ¿Cuántas moléculas de H2 (hidrógeno) y O2 (oxígeno) necesitamos para hacer exactamente 2 moléculas de agua sin que haya excedente?
PREDICCIÓN: comprobación:
10) Escribí la reacción química BALANCEADA de formación del agua. Es decir, escribila en forma de ecuación y redactala con tus palabras.
¡Ahora pueden seguir practicando de la misma manera con las otras reacciones químicas!
Fíjense cuántos productos pueden obtener con diferentes cantidades de cada uno de los reactivos para cada una de las reacciones químicas que les propone el simulador: 1- hacer agua, 2- hacer amoníaco, y 3- quemar metano. Presenten atención a las ecuaciones químicas que representan cada una de estas transformaciones químicas. ¿Estas ecuaciones están balanceadas? Sí, noten que delante de cada una de las sustancias aparecen números que llamamos coeficientes estequiométricos para balancear las ecuaciones. También pueden comprobar si se cumple el principio de conservación de la materia para chequear que las reacciones están balanceadas. Si tienen ganas de seguir practicando, pueden utilizar el modo JUEGO del simulador.
11. Autoevaluación
Para seguir pensando y practicando los conceptos que vimos en este bloque, te proponemos realizar la siguiente actividad de auto-evaluación, a la que pueden acceder haciendo clic en Cuestionario..
|
Si no tenés un usuario creado en este campus no podés hacer las autoevaluaciones. Te dejamos las instrucciones para poder realizarlas:
|