Estructura atómica
6. Masa atómica
¡Sigamos trabajando con la Tabla Periódica de los Elementos! Como se mostro en el video anterior, debajo del NOMBRE de cada ELEMENTO figura la MASA ATÓMICA: es decir, la masa de los átomos que pertenecen a ese elemento. Debemos aclarar que no es la masa de un átomo en particular, sino el PROMEDIO de la masa de los distintos isótopos que se encuentran en la naturaleza para cada elemento, TENIENDO EN CUENTA SU ABUNDANCIA RELATIVA. Deberíamos llamarla MASA ATÓMICA PROMEDIO, pero en la práctica la llamamos MASA ATÓMICA. Veamos un ejemplo:
El cloro tiene dos isótopos: Cl-35 y Cl-37. Si la masa atómica del cloro fuese simplemente el promedio de masas de sus isótopos 35 y 37, sería 36 no? Pero si se fijan en la tabla periódica la masa atómica del Cloro es 35,45. ¿Por qué? La respuesta tiene que ver con el hecho que diferentes isótopos tienen distinta abundancia relativa, es decir que algunos isótopos naturalmente son más abundantes en la Tierra que otros. En el caso del cloro, el cloro-35 tiene una abundancia relativa de 75,5% mientras que el cloro-37 tiene una abundancia relativa de 24,5%. Observa que la abundancia relativa es un porcentaje y por lo tanto la abundancia relativa de todos los isótopos estables distintos de un elemento suman 100%.
Entonces, teniendo en cuenta su abundancia relativa calculamos el promedio ponderado de masas atómicas de los isótopos del cloro de la siguiente manera= 35 uma x 75,5/100 + 37 uma x 24,5/100 = 35,45 uma. Esta masa atómica es la que apareceen la tabla periódica para el cloro.
¡Ojo! Si bien son palabras similares no es lo mismo el NÚMERO MÁSICO y la MASA ATÓMICA.
En la Tabla Periódica NO se indica el número másico (que corresponde a la suma de protones más neutrones y por lo tanto SIEMPRE ES UN NÚMERO ENTERO); en cambio, SÍ se indica la masa atómica que, como vimos es un promedio de la masa de todos los isótopos teniendo en cuenta su abundancia relativa, por eso se trata siempre de un número con decimales. ESTE VALOR SÍ LO PODEMOS ENCONTRAR EN LA TABLA PERIÓDICA, como pueden ver en la siguiente imagen:
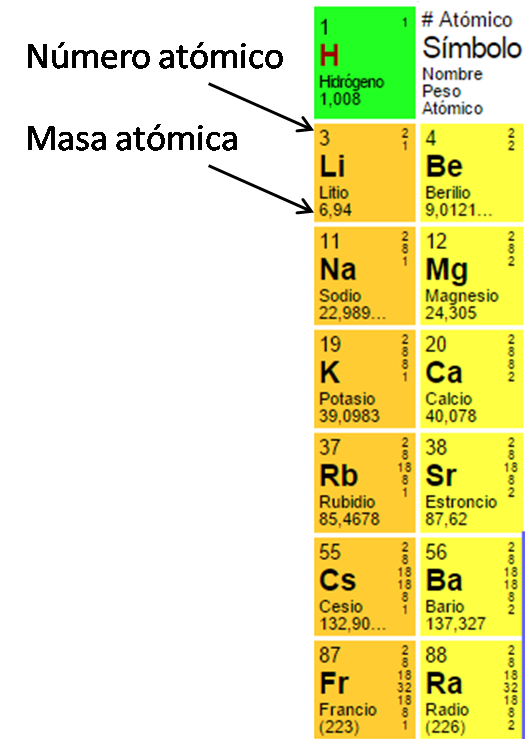
Tengan en cuenta que como las partículas subatómicas que aportan a la masa de los átomos son los NEUTRONES y los PROTONES y su masa es 1 uma, en general la MASA ATÓMICA de un átomo suele ser un número muy cercano a su NUMERO MÁSICO.
También es importante notar que las masas de los átomos son muy pequeñas comparadas con las masas que manejamos habitualmente. Esto hace imposible medirlas con las balanzas convencionales y en las unidades habituales como kg, g e incluso mg que resultan demasiado grandes para que sean de utilidad. Este tema se verá en profundidad en otro bloque, pero te adelantamos que como NO es posible pesar un solo átomo con ningún instrumento hasta la fecha. Por eso para determinar la masa de los mismos, se tomo como PATRÓN de referencia al isótopo más abundante del carbono (C-12), asignando a su masa un valor de doce unidades de masa atómica (uma). Por lo tanto, las masas atómicas tal como figuran en la Tabla periódica corresponden a masas atómica relativas (que se abrevia como Ar). Al ser relativas, estos números indican cuantas veces es mayor la masa de un átomo en relación a la unidad de masa atómica. Veamos un ejemplo:
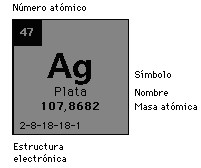
Por ejemplo, la masa atómica de la plata es 107,8682 (sin unidades), es decir, que un átomo de plata es 107,8682 veces más pesado que 1 uma o que un átomo de plata pesa 107,8682 uma.
