Clasificación periódica
3. Organización de los Elementos en la Tabla Periódica.
En la Tabla Periódica actual los elementos químicos se encuentran ordenados de acuerdo con su numero atómico (Z) creciente de izquierda a derecha y de arriba hacia abajo. Los elementos presentes en la Tabla se pueden clasificar de diferentes maneras, que veremos a continuación.
La Tabla actualmente está organizada en:
- grupos (18 columnas) que se numeran del 1 al 18, o con números romanos y un letra A o B,
- períodos (8 filas) numerados de 1-8.
Los elementos que están en el mismo grupo (es decir, en la misma columna) tienen igual número de electrones de valencia, que son los electrones que están en el orbital más externo y los que participarán de las uniones químicas (tema que desarrollaremos en otro bloque). Por esa razón los elementos de un mismo grupo, es decir que están en una misma columna, presentan propiedades químicas semejantes, y se dice que forman parte de una misma FAMILIA. Algunas de estas familias tienen nombres propios, como por ejemplo:
- los elementos del grupo IA o 1 que se llaman Metales Alcalinos,
- los del grupo IIA o 2 que se denominan Metales Alcalinos Térreos,
- los del grupo VIIA o 17 que son los llamados Halógenos,
- los del grupo VIIIA o 18 son llamados Gases Nobles o Inertes.
Como dijimos anteriormente en la Tabla los elementos están ordenados por su Z (número atómico), desde el elemento de Z = 1 (Hidrógeno) en adelante (leyendo de izquierda a derecha y de arriba hacia abajo) y se pueden clasificar de distintas maneras. Una de las formas más comunes de clasificación es según sus propiedades químicas como:
- Metales,
- No metales y
- Metaloides.
Una ACLARACIÓN IMPORTANTE: si bien el Hidrógeno está ubicado en el grupo 1 o IA, NO es un metal alcalino. El Hidrógeno es un NO METAL, pero esta ubicado allí porque su Z= 1. En la imagen de abajo pueden ver cómo a los elementos coloreados según esta clasificación:

Existe también otra clasificación de los elementos según el subnivel (s, p, d ó f) en el que ingresa el electrón diferencial; esto es, como los elementos están ordenados según su número atómico, cada elemento difiere del anterior por un protón y por ende por un electrón que se denomina electrón diferencial. Siguiendo esta regla los elementos se clasifican en:
- Elementos Representativos, los que ubican su electrón diferencial en el subnivel s o p;
- Elementos de Transición, los que ubican su electrón diferencial en el subnivel d,
- de Transición Interna, los que ubican su electrón diferencial en el subnivel f.
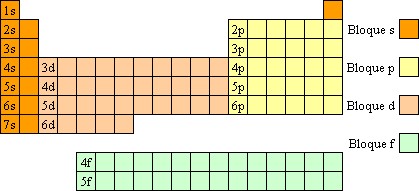
Existen los bloques:
s que abarca los grupos 1 y 2 y el elemento He;
p que abarca los grupos
d que abarca los grupos
f que abarca dos filas, la de los lantánidos y los actínidos.
Como se mencionó antes, este criterio permite clasificar los elementos en: representativos, de transición y de transición interna, como se muestra en el esquema de abajo:
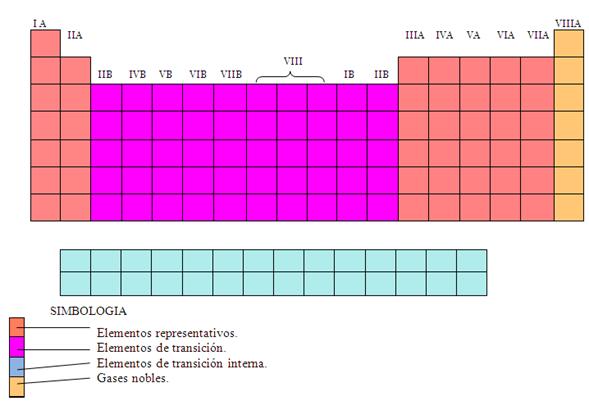
Así la distribución de familias de elementos dentro el sistema periódico es:
• Elementos representativos formados por:
Alcalinos: Grupo IA;
Alcalinotérreos: Grupo IIA Térreos;
Boroideos: Grupo IIIA;
Carbonoideos: Grupo IVA;
Nitrogenoideos: Grupo VA;
Anfígenos: Grupo VIA;
Halógenos: Grupo VIIA;
Gases nobles o inertes: Grupo VIIIA.
• Elementos de transición formados por los grupos IIIB, IVB, VB, VIB, VIIB, VIIIB (que incluye tres columnas), IB y IIB. Se sitúan en el centro del Sistema Periódico.
• Elementos de transición interna formados por las familias de Lantánidos y Actínidos, de 14 elementos cada una. Se colocan en dos filas habitualmente fuera del entorno general.
• El hidrógeno queda fuera de estas consideraciones, y por tener un solo electrón que está alojado en el orbital 1s, se coloca encima del grupo de Alcalinos IA.
