Uniones químicas y propiedades de las sustancias
4. ¿De qué depende el tipo de unión que ocurre entre los átomos?
Para entender de qué depende que los átomos se enlacen por medio de uniones iónicas o covalentes, repasemos dos propiedades de los átomos que vimos en el bloque llamado ¨Clasificación Periódica¨: la electronegatividad y la energía de ionización.
Existen átomos como los no metales (especialmente el nitrógeno, el oxígeno y los halógenos (elementos del grupo 17: F, Cl, Br, I) que tienen una tendencia fuerte a atraer electrones ya que presentan altos valores de electronegatividad y alta energía de ionización. Fíjense que a todos ellos les faltan pocos electrones para completar el octeto (tienen 7 electrones en su orbital más externo y sólo les falta 1 electrón para completar el octeto). En cambio, los metales alcalinos y alcalinos térreos presentan bajas electronegatividades y baja energía de ionización, por lo tanto tienen tendencia a perder electrones fácilmente. Si estos elementos pierden los pocos electrones de valencia que tienen (1 ó 2) alcanzan la configuración del gas noble más cercano y quedan con la capa completa (con 8 electrones en su último orbital).
Teniendo en cuenta esto, ¿por qué algunos átomos forman enlaces covalentes y otros forman enlaces iónicos o metálicos?
Veamos. Si dos elementos tienen baja tendencia a perder sus electrones (alta energía de ionización) y tienen tendencias parecidas a atraer electrones (electronegatividades similares) van a compartir electrones y formar enlaces covalentes. Ninguno de los átomos va a querer perder sus electrones pero están interesados en completar el octeto: mejor compartir. Estos elementos por lo general son no metales. Por lo tanto, los no metales tienden a formar enlaces covalentes entre ellos.
En cambio, si tenemos un elemento con mucha tendencia a formar cationes (baja energía de ionización) como un metal alcalino y otro que tiende a atraer electrones (alta electronegatividad) como un no metal, seguramente ocurra una transferencia de electrones: el metal alcalino le cede sus electrones al no metal. El metal forma un catión y el no metal un anión, que se atraen fuertemente entre sí porque sus cargas eléctricas son contrarias. El enlace que se forma entonces es un enlace iónico. Los metales tienden a formar enlaces iónicos con los no metales.
Si tenemos muchos átomos metálicos, como en una pieza de metal, todos van a tener una tendencia considerable a perder sus electrones y formar cationes (energías de ionización bajas). Forman entonces lo que llamamos un enlace metálico. Los átomos que forman una pieza de metal están en la forma de cationes. Sus electrones de valencia están débilmente unidos y no están asociados a ningún átomo metálico en particular. Recuerden que los metales tienen baja tendencia a atraer electrones en un enlace (tienen baja electronegatividad). Son compartidos por toda la pieza de metal, por todo el "cristal metálico".
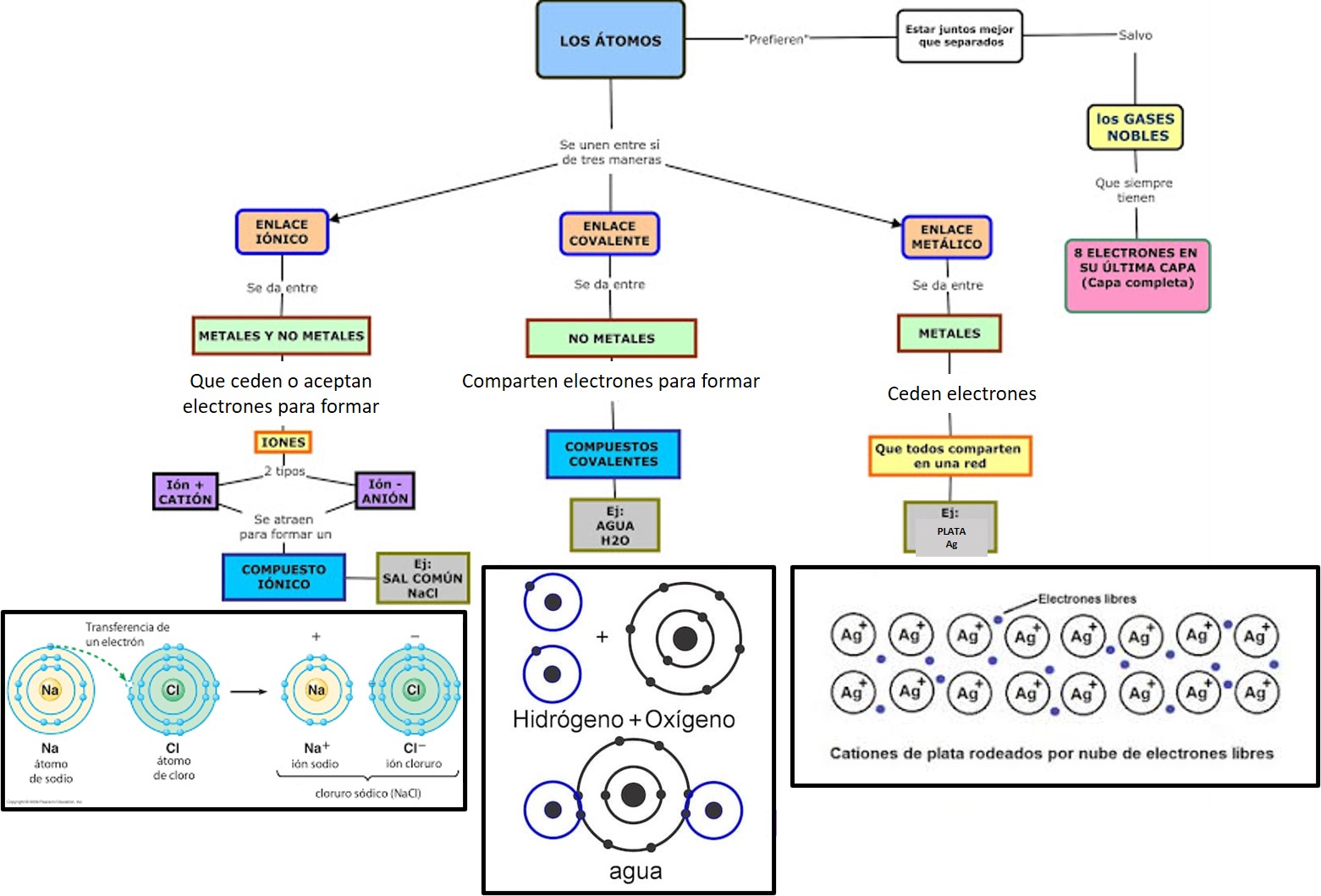
En el siguiente cuadro sinóptico se sintetizan las principales características de estos tres tipos de enlaces químicos: