Uniones químicas y propiedades de las sustancias
5. ¿Cuál es la relación entre la estructura química y las propiedades que presentan las sustancias?
Hasta aquí aprendimos que existen 3 tipos principales de uniones químicas entre los átomos que dan lugar a todas las sustancias y cosas que conocemos: UNIONES IÓNICAS que forman SALES, UNIONES COVALENTES que ocurren en las moléculas y UNIONES METÁLICAS presentes entre los metales. Como dijimos anteriormente, para poder interpretar y/o predecir las propiedades de las diferentes sustancias, debemos conocer a qué tipo pertenecen. En adelante vamos a examinar la relación entre la estructura química y las propiedades que presentan las sustancias.
Habitualmente usamos sustancias que tienen propiedades muy diferentes. A temperatura ambiente, la sal, el azúcar y el cobre son sólidos, el agua y el alcohol son líquidos, el oxígeno, el dióxido de carbono, el metano y el amoníaco son gases.
Si bien la sal y el azúcar comparten algunas propiedades -como ser sólidos cristalinos, blancos y solubles en agua-, no comparten otras, como la temperatura a la cual funden. Si calentamos suavemente azúcar en una cacerola, funde fácilmente, obteniéndose el conocido “caramelo”. En cambio, no podemos transformar la sal sólida en sal líquida con el calor que genera el fuego de la hornalla, porque la temperatura de fusión del NaCl es mucho mayor que la temperatura de fusión de la sacarosa, nombre químico del azúcar común, C12H22O11 y que la que se alcanza con la llama de la hornalla. Por otra parte, estas sustancias casi no comparten propiedades con el cobre, más allá de ser sólidas a temperatura ambiente.
El oxígeno, el amoníaco, el metano y el dióxido de carbono son sustancias gaseosas a temperatura ambiente; pero sus propiedades son bien distintas. El olor picante y desagradable del amoníaco, NH3, es muy característico; en cambio, el oxígeno, O2, no tiene olor. El metano, CH4, es un combustible, mientras que el dióxido de carbono, CO2, es un producto de la combustión. El oxígeno favorece la combustión mientras que el CO2 se utiliza para lo contrario, en los extintores contra incendios (matafuegos).
¿Dónde radica la causa de las semejanzas y las diferencias en el aspecto y comportamiento de las distintas sustancias? Comencemos por analizar qué ocurre durante los cambios de estado:
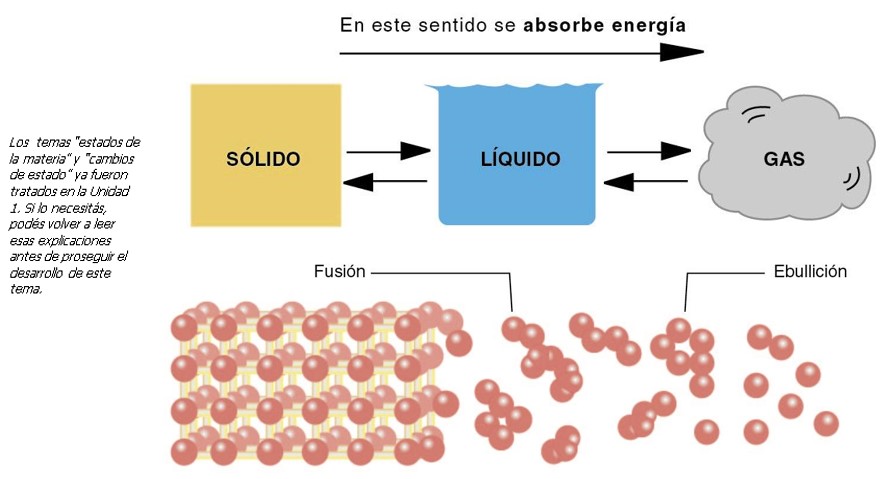
Para que se produzca el pasaje de una sustancia del estado sólido al estado líquido (recordà que dicho cambio se denomina fusión), es necesario entregar energía (generalmente en forma de calor) a dicha sustancia para “vencer” las fuerzas de atracción que mantienen a sus partículas vibrando alrededor de determinadas posiciones (estado sólido), y que así puedan deslizarse unas sobre otras (estado líquido).
Algo similar sucede durante la vaporización: debemos entregar energía suficiente para que las partículas de un líquido logren separarse disminuyendo, entonces, la intensidad de las fuerzas de atracción entre ellas. Cuanto más intensas sean las interacciones que hay entre las partículas, mayor cantidad de energía será necesaria para separarlas y, por lo tanto, mayor será la temperatura a la que ocurre el cambio de estado.
Por lo tanto, el estado de agregación de una sustancia a una temperatura dada depende de la intensidad de las fuerzas que hay entre las partículas que lo forman.
Las SUSTANCIAS IÓNICAS O SALES forman CRISTALES como los que se ven en la imagen de abajo, donde se alternan CATIONES y ANIONES en la estructura, unidos por fuerzas eléctricas intensas entre las cargas positivas y negativas. La fórmula química indica la proporción de los componentes del cristal. Por ejemplo, un cristal de cloruro de sodio tiene la siguiente fórmula química: NaCl, que indica que por cada catión Na+ hay un anión Cl-. Las fuerzas que mantienen la estructura de cristal son las fuerzas de la unión iónica. Las sales son SÓLIDAS a temperatura ambiente:

Las SUSTANCIAS METÁLICAS o METALES también formaban cristales como se ve en esta otra imagen, por eso la mayoría de los metales son SÓLIDOS a temperatura ambiente, a excepción del Hg (mercurio):

Ahora bien, las sustancias en las que los átomos se enlazan por UNIONES COVALENTES forman MOLÉCULAS. En este caso, la fórmula química indica cómo está compuesta la molécula. Por ejemplo, el gas Cl2 está formado por unidades de Cl-Cl, es decir, moléculas en las que hay dos cloros unidos por un enlace covalente simple. Las sustancias como el gas Cl2, el dióxido de carbono (CO2), el agua (H2O), el metano (CH4), el etanol (C2H6O) o el azúcar de mesa (C12H22O11) están formadas por moléculas. En cada molécula, los átomos se mantienen unidos por enlaces covalentes y a su vez las moléculas se encuentran unidas entre sí por otras fuerzas, que llamamos fuerzas intermoleculares (ENTRE moléculas). Estas fuerzas son muy débiles en el gas Cl2 o en el CO2, por lo que estas sustancias se encuentran en forma de gases a temperatura ambiente. En el agua, el etanol o el azúcar de mesa, las fuerzas intermoleculares son más intensas y por lo tanto, las moléculas logran mantenerse unidas formando un líquido en el caso del agua y el etanol, y un sólido en el caso del azúcar a temperatura ambiente. Como ven el estado de agregación (sólido, líquido o gaseoso) en las sustancias moleculares depende fundamentalmente de la INTENSIDAD O MAGNITUD de las fuerzas entre sus moléculas. La magnitud de estas fuerzas a su vez depende de la geometría (distribución de los átomos de la molécula en el espacio), tamaño de la molécula y distribución de sus cargas. En la imagen de abajo se muestra en forma esquemática la geometría de distintas moléculas:
