Soluciones
3. Solubilidad
Se denomina solubilidad a la concentración de la solución saturada a una presión y temperatura dada. La solubilidad se expresa generalmente como gramos (g) de soluto/100g de solvente o g de soluto/100 ml de solvente.
La solubilidad de los sólidos en los líquidos siempre es limitada y depende de la naturaleza del soluto, del solvente, de la temperatura principalmente y muy poco de la presión. Esto quiere decir, por ejemplo, que si estamos disolviendo sal de mesa (NaCl) en agua (como se muestra en la figura de abajo), no podemos agregar sal (soluto) indefinidamente al agua (solvente). En el primer ejemplo se agregan 25 g de sal a 100 mL de agua, y se obtiene una solución NO SATURADA o INSATURADA (donde todo el soluto se disuelve en el solvente). Sin embargo, si seguimos agregando sal, en un punto, cuando lleguemos al límite de saturación, esa dada cantidad de agua (solvente) ya no podrá disolver la sal y se formará un precipitado en el fondo del vaso (es decir que quedara la sal en forma sólida en el fondo del vaso). Esto es lo que ocurre en el segundo caso que muestra la imagen de abajo: al tratar de disolver 50 g de sal en 100 mL de agua se obtiene una solución SATURADA; en esta solución 36 g de sal se disuelven y 14 g de sal no se disuelven y quedan en el fondo del vaso en forma de precipitado.
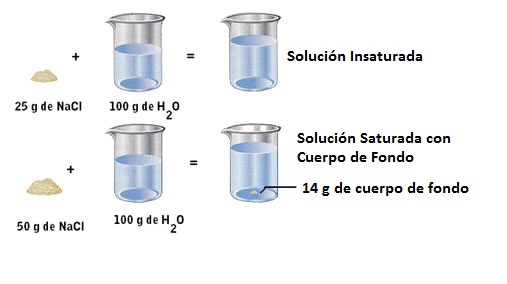
Como dijimos antes, en el caso de la solubilidad de los sólidos en los líquidos, la Temperatura es condicionante de dicha solubilidad, pero no tanto la Presión.
En cambio, si estamos considerando la solubilidad de los gases en líquidos tanto la presión como la temperatura deben tenerse en cuenta: en este caso la solubilidad aumenta con la presión y disminuye con la temperatura. ¿Qué ejemplos de la vida cotidiana se les ocurren? Piensen qué ocurre con el gas al destapar una botella de gaseosa o al hervir agua...
