Soluciones
4. Soluciones Saturadas versus Soluciones no saturadas
Como mencionamos previamente, existe una cantidad máxima de soluto sólido que se puede disolver en un determinado volumen de solvente líquido a una determinada temperatura antes de que el sistema se transforme en heterogéneo. A esto se llama límite de saturación. Teniendo en cuenta el límite de saturación, las soluciones se pueden clasificar en SOLUCIONES SATURADAS Y NO SATURADAS.
Las SOLUCIONES SATURADAS son aquellas que presentan una cantidad mayor a la máxima cantidad de soluto que puede disolverse en un determinado volumen de solvente a una dada temperatura, es decir que alcanzaron o superaron el límite de saturación. El límite de saturación es la máxima cantidad de soluto que puedo disolver en un determinado volumen de solvente a una cierta temperatura y presión.
Pensemos en la siguiente situación: si tratamos de disolver azúcar en un vaso de agua (que tiene 200 mL de agua), ¿podremos agregar azúcar indefinidamente, mezclar y siempre observar que el azúcar se disuelve? No, esos 200 ml de agua son capaces de disolver una cierta cantidad de azúcar, pero el exceso de soluto que no pudo disolverse va a precipitar. Entonces el sistema se transformará en heterogéneo, porque al precipitar el exceso de soluto en las soluciones saturadas se observan dos fases: el soluto precipitado en el fondo y la solución saturada de azúcar y agua por encima. Las soluciones saturadas están en un equilibrio dinámico con un exceso de soluto sin disolver. En el equilibrio dinámico, las velocidades de precipitación y de disolución del soluto son iguales, como se muestra en la imagen de abajo. Poniéndonos un poco más técnicos: se denomina solución saturada a aquella que está o puede estar en equilibrio dinámico con un exceso del soluto sin disolver.
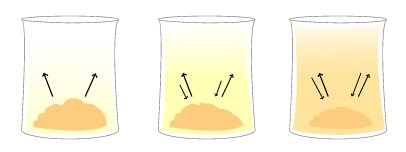
- Al colocar un soluto en agua comienza a disolverse;
- La velocidad de disolución es mayor que la de precipitación (observá el tamaño de las flechas);
- Se llega a un equilibrio dinámico: las velocidades de disolución y precipitación son iguales.
En cambio en las SOLUCIONES NO SATURADAS, la cantidad de soluto disuelto es menor al límite de saturación, esto quiere decir, que es menor a la máxima cantidad de soluto que admite esa cantidad de solvente.
Se suele utilizar una distinción entre soluciones diluidas (donde la cantidad de soluto disuelto es mucho menor que el límite de saturación) y soluciones concentradas (donde la cantidad de soluto disuelto es cercana al límite de saturación), pero esta última clasificación es un tanto grosera y es sólo cualitativa. Con esto queremos decir que puede ser útil para comparar soluciones y establecer cuándo una solución es más o menos concentrada que otra, pero no nos da información para identificar inequívocamente una solución particular. Por ejemplo, como se ve en la figura de abajo las dos soluciones del medio no se pueden identificar inequívocamente:
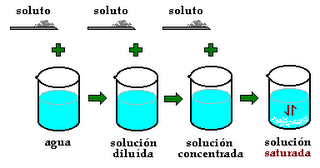
Siempre que tengamos un sistema heterogéneo, como en el caso de la solución saturada, y no haya disminución de la cantidad de soluto en el fondo (o aumento en la intensidad del color de la solución) con el tiempo, podemos afirmar que la solución que se observa sobre el residuo sólido del fondo está saturada.
Si tenemos un sistema homogéneo, es decir que no hay exceso de soluto en el fondo, sólo podemos comprobar que la solución está saturada agregando una pequeñísima cantidad de soluto y viendo si se disuelve (con lo cual sería no saturada) o si no se disuelve y precipita en el fondo (ya estaría saturada, porque no admite más soluto en solución). La otra manera es preparar la solución con los datos de las tablas de solubilidad y disolver exactamente la cantidad de soluto necesaria para la saturación.
A MODO DE RESUMEN...
- Se denomina solubilidad a la concentración de la solución saturada a una presión y temperatura dada.
- La solubilidad se expresa generalmente, en g de soluto/100g de solvente ó g de soluto/100 ml de solvente.
- La solubilidad varía con la temperatura y la presión.
- La solubilidad de los sólidos en los líquidos es siempre limitada y depende de la naturaleza del solvente, de la del soluto, de la temperatura y muy poco de la presión.
- La presión tiene una gran importancia cuando se consideran solubilidades de gases.
- La solubilidad de los gases aumenta al disminuir la temperatura.
- La solubilidad de los gases aumenta al aumentar la presión.
