Reacciones químicas y cálculos estequiométricos
5. ¿Cómo se leen las ecuaciones químicas?
Analicemos un poco más en detalle la ecuación anterior...
4 Fe + 3 O2 ----------------> 2 Fe2O3
En esta reacción en términos CUANTITATIVOS lo que ocurre es que:
4 átomos de Hierro (Fe) reaccionan con 3 moléculas de Oxígeno (O2) para formar 2 unidades fórmula de Óxido de Hierro (Fe2O3).
Pero, ¿normalmente hablamos de las sustancias que reaccionan en términos de moléculas y átomos? ¿Se puede pesar en una balanza convencional la masa de 1 átomo?
Las respuestas a las preguntas planteadas arriba es NO. No se puede pesar en una balanza convencional la masa de 1 átomo o 1 molécula. La masa de los átomos y las moléculas son muy pequeñas comparadas con las masas que manejamos habitualmente.
Esto hace imposible medirlas con las balanzas convencionales y en las unidades habituales como kg, g e incluso mg que resultan demasiado grandes para que sean de utilidad.
Tanto en nuestra vida diaria como en el laboratorio usamos muestras de sustancias que contienen una enorme cantidad de átomos, moléculas o iones. Como ya dijimos, estas partículas tienen masas muy pequeñas y no existen balanzas que puedan pesarlas en forma individual. Por lo tanto, es conveniente utilizar una unidad especial que sirva para describir una cantidad de átomos o moléculas muy grande. Esta unidad es el MOL.
Un mol es una unidad que emplean los químicos para describir una cantidad muy grande de átomos o moléculas. Así como una docena se refiere a 12 unidades (de huevos, facturas, etc.) o 1 centena se refiere a 100 unidades (de alfajores, bolillas, etc.),
1 mol corresponde a 6,02. 1023 partículas (átomos o moléculas o iones),
siendo 6,02. 1023 igual a
602.000.000.000.000.000.000.000
Por definición, 1 mol equivale al número de átomos que hay en 12 g de Carbono de A= 12.
Entonces, en 1 mol hay siempre 6,02. 1023 (este número se llama número de Avogadro o constante de Avogadro) partículas; en nuestro caso serán moléculas o átomos o iones. Notar que NO estamos hablando de 1 molécula o 1 átomo, sino de moles, es decir un número muy grande, que describe ¡millones de átomos o moléculas!
¿Cómo se calcula la masa de un mol de sustancia?
La masa de 1 mol de átomos o 1 mol de moléculas coincide numéricamente con su Ar (masa atómica relativa, que figura en la Tabla Periódica de los Elementos para cada tipo de elemento) o con su Mr (masa molecular relativa) que resulta de la suma de las masas atómicas de los átomos que forman la molécula, pero lleva unidad de gramos.
Esto es un lio de palabras nuevas, lo sé, pero miren los ejemplos que siguen y van a ver que es más fácil de lo que parece.
¿Cómo calculo la masa de un mol de átomos?
Fíjense, dijimos que la masa de un mol de átomos es numéricamente igual a la masa atómica relativa (Ar) pero lleva unidad de gramos.
Por ejemplo:
Ar Na = 23 y la masa molar (la masa de un mol de átomos) de Na es igual a 23 g.
¿Y cómo calculo la masa de un mol de moléculas?
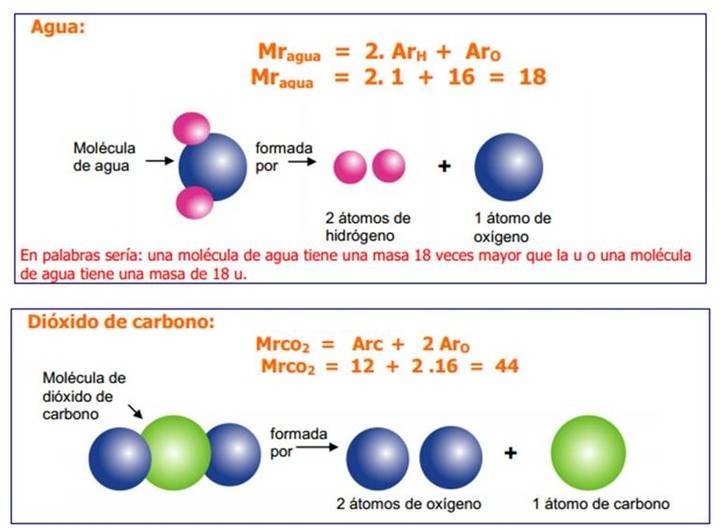
La masa de un mol de moléculas es numéricamente igual a su masa molecular relativa (Mr), que puede determinarse sumando las masas atómicas de los elementos que la componen, pero lleva unidad de gramos.
Por ejemplo:
Mr del agua = 18, y la masa molar del agua es igual a 18 g.
Mr del dióxido de carbono = 44, y la masa molar del dióxido de carbono es igual a 44 g.