Reacciones químicas y cálculos estequiométricos
7. Reacciones de Combustión
Como vimos previamente, durante las reacciones químicas se rompen enlaces químicos (que mantienen unidos a los átomos o iones en las moléculas o compuestos iónicos) en las sustancias que reaccionan (llamados reactivos), éstos se reordenan y forman nuevos enlaces que darán origen a sustancias distintas (que serán los productos). Las reacciones químicas se representan por medio de ecuaciones químicas; en estas solo se indica globalmente lo que está ocurriendo en la reacción.
También dijimos que para que las ecuaciones químicas estén correctamente escritas deben estar siempre correctamente balanceadas. Tanto en la combustión como en la respiración se produce una reacción química donde uno de los reactivos es el oxígeno (O2), por eso este tipo de reacciones se denominan oxidaciones.
Ahora bien, ¿qué reactivos son necesarios para que se produzca una combustión?
En primer lugar se necesita un combustible, la sustancia que arde o se quema, por ejemplo la madera. En la imagen de abajo pueden ver distintos tipos de combustibles:

¿Qué otros combustibles utilizas con frecuencia? Escribí en tu cuaderno 3 ejemplos.
Pero con el combustible solo no alcanza, ¿qué más se necesita para que el combustible resulte útil y se produzca una reacción de combustión?
Para ayudarte a responder te proponemos que realices el siguiente experimento:
1. Encende una vela y obsérvela al comenzar y luego de varios minutos.
¿Qué se quema de la vela, la cera o el pabilo?
2. Tapa la vela con un vaso de vidrio y encendé una segunda vela, de la siguiente manera:
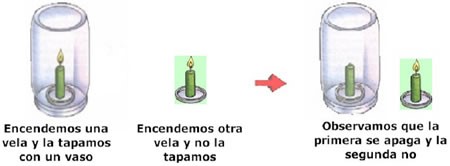
Responde:
¿Qué ocurre con la vela que está tapada con el vaso luego de unos minutos?
Observe las paredes del vaso. ¿Cómo están? ¿Por qué se apaga la vela si se le quita el aire?
Las actividades realizadas, junto con tu experiencia con diferentes formas de combustión, te habrán llevado a algunas conclusiones importantes respecto del proceso que estamos analizando. Para que se produzca la combustión, se necesita no sólo un combustible sino además aire que provee el comburente, la sustancia que permite que se produzca la combustión, y una temperatura de ignición (en el caso de la vela, dada por el fósforo encendido) para que el sistema combustible-comburente llegue a la temperatura necesaria para continuar por sí solo la reacción. Se dice que un material combustible es más inflamable que otro si comienza a arder a una temperatura más baja.
Podemos entonces concluir que la combustión requiere la presencia de aire, tal como lo necesita un ser vivo para respirar. Estos resultados nos hacen pensar que puede haber cierta semejanza entre la respiración y la combustión...
No cabe duda, el aire juega un importante papel en estos procesos; pero, en realidad, ¿es todo el aire o sólo una parte de él, la que interviene en los procesos de respiración y de combustión? Al apagarse la vela, ¿no quedó nada de aire en el frasco?, ¿todo el aire que contenía el frasco se gastó en la combustión de la vela?
Es posible responder a estas preguntas, y comprobar mediante experimentos que se ha consumido tan solo una parte del aire que estaba encerrado en el frasco: se trata del oxígeno (cuya fórmula molecular es O2), uno de los componentes de la mezcla gaseosa que denominamos aire.
Como productos de las reacciones de combustión en general, se obtienen agua, dióxido de carbono (CO2) y energía lumínica (luz) y térmica (calor). En forma general podemos escribir una ecuación para las reacciones de combustión de la siguiente manera:
COMBUSTIBLE + COMBURENTE -------> PRODUCTOS + ENERGÍA
En conclusión:
- Combustible es toda sustancia capaz de arder en presencia de oxígeno;
- La respiración y la combustión son procesos en los que se produce una reacción química con el oxígeno, en términos químicos se las llama reacciones de OXIDACIÓN;
-
En la combustión se libera una importante cantidad de energía, que se transfiere a otros sistemas en forma de calor. Por eso se dice que se trata de un proceso exotérmico (exo: hacia fuera; térmico: calor). De manera general cuando se libera energía en cualquier forma que sea, el proceso se denomina exergónico.
